2023年8月14日に発表された、サスメド株式会社2023年6月期決算説明の内容を書き起こしでお伝えします。
スピーカー:サスメド株式会社 代表取締役社長 上野太郎 氏
サスメド株式会社 取締役 小原隆幸 氏
ビジョン
上野太郎氏(以下、上野):サスメド株式会社の上野です。本日はお忙しい中、お集まりいただきありがとうございます。それでは、2023年6月期の決算説明を始めます。
まずは弊社の紹介です。弊社は「ICTの活用で『持続可能な医療』を目指す」をビジョンに掲げており、その意味である「SUStainable MEDicine」を略して、サスメドと称しています。
具体的な取り組みについてご説明します。1つはDTx(Digital Therapeutics)プロダクト事業で、医療機器である治療用アプリを、疾患ごとに患者や医療従事者に提供しています。
もう1つはDTxプラットフォーム事業です。治療用アプリを効率よく開発するためのローコードツールや、ブロックチェーン技術を使用した臨床試験の効率化を図るシステムを開発しています。こちらは治療用アプリに限らず、医薬品の開発でも活用できますが、製薬企業などに向けBtoBで提供しています。
事業領域概要
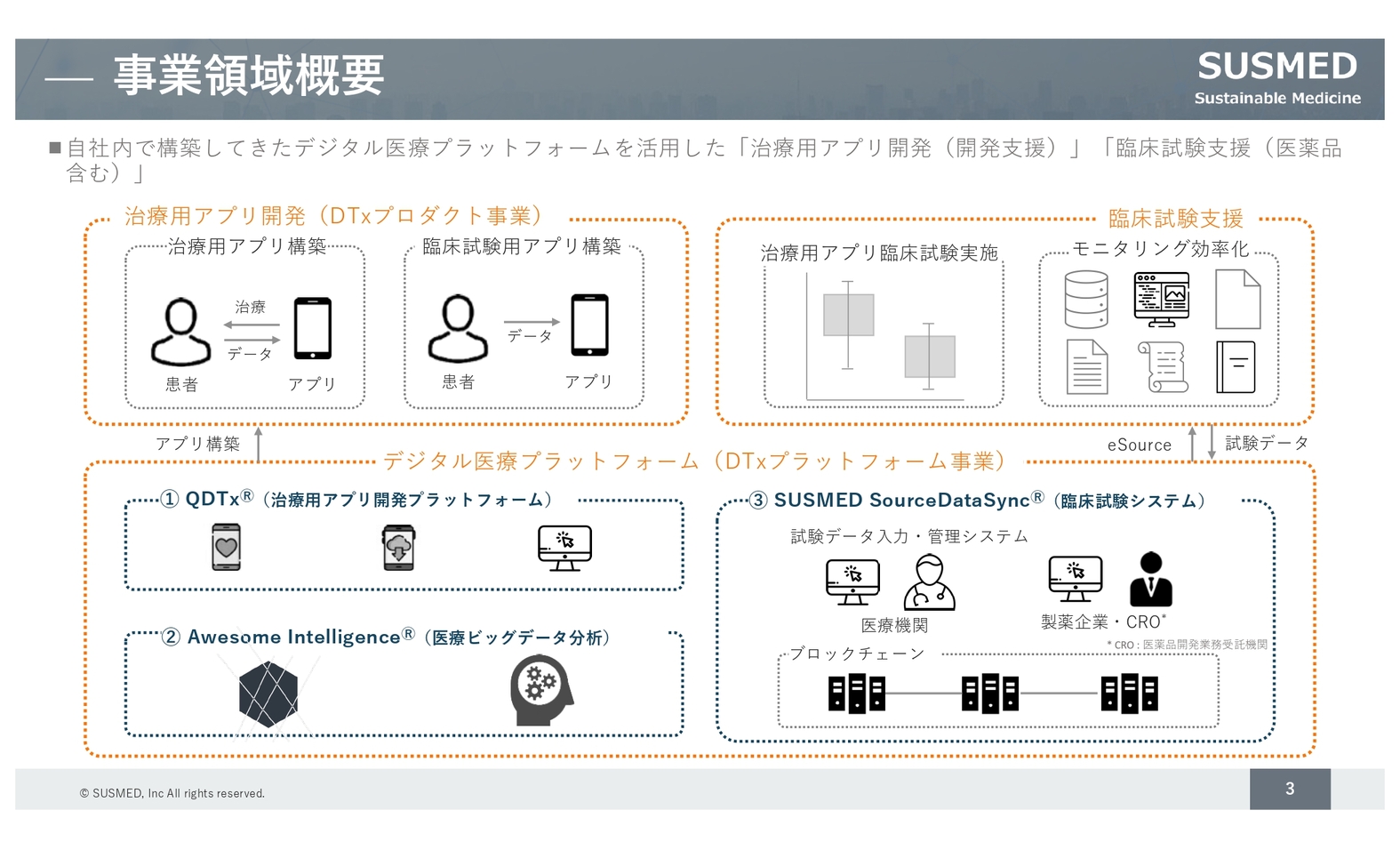
事業概要です。弊社は、不眠障害治療用アプリの開発を目的として創業しました。現在は、がん患者向けのアプリや腎臓病患者向けのアプリなど、さまざまな治療用アプリを開発しています。また、医薬品も含めた臨床試験の効率化を図る事業も展開しています。
この2つの事業を支える弊社の知財が、スライド下部に記載しているデジタル医療プラットフォームです。具体的には、3つのプラットフォームがあります。1つ目が「Q(クイック)DTx」で、治療用アプリを効率良く開発するためのプラットフォームです。こちらはローコードツールのため、臨床試験までを効率よく進めることができます。
2つ目は「Awesome Intelligence」で、医療ビッグデータを分析するためのクラウドサービスです。
3つ目は「SUSMED SourceDataSync」です。こちらはブロックチェーン技術を組み込むことで、治験を効率よく、かつレギュレーション対応しながら実施できる臨床試験の管理システムです。
治療用アプリの提供の流れ
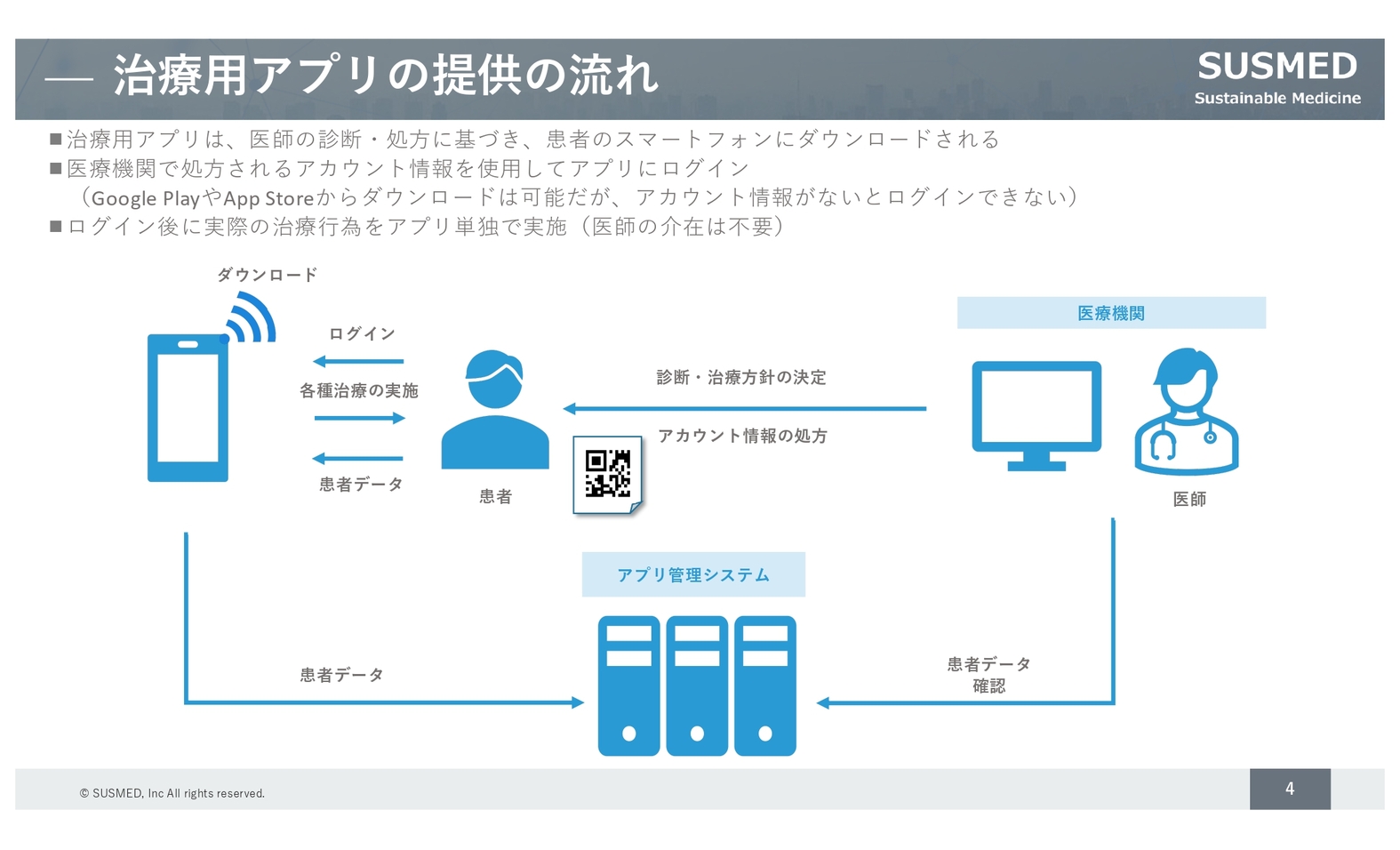
治療用アプリはこれから普及していく段階にあるため、提供の流れについてあらためてご説明します。治療用アプリは医療機器に該当しますので、薬や医療機器と同じ流れで提供されます。
したがって、医師の診断・処方により初めて患者が使えるようになります。お薬の場合は処方箋が渡されますが、治療用アプリの場合はログインするためのアカウントが処方され、そのアカウントを使用して患者がログインすることで治療用アプリを使うことができるようになる仕組みです。
治療用アプリは遠隔診療と大きく異なり、単独で治療が行えるのが特徴です。遠隔診療の場合は裏側に医師が必要になるため、医療機関側の労力はあまり変わりません。しかし治療用アプリの場合は、アカウントを発行した後はアプリ単独で治療できますので、まさにお薬と同じような扱いで医療機関側の追加の負担はありません。
既存の医薬品と治療用アプリとの大きな違いは、患者のデータが日々生み出されることです。サーバーに収集される治療用アプリのデータを確認し、治療方針の策定に活用できることも、新しいポイントになっています。
ヘルスケアアプリと治療用アプリの違い
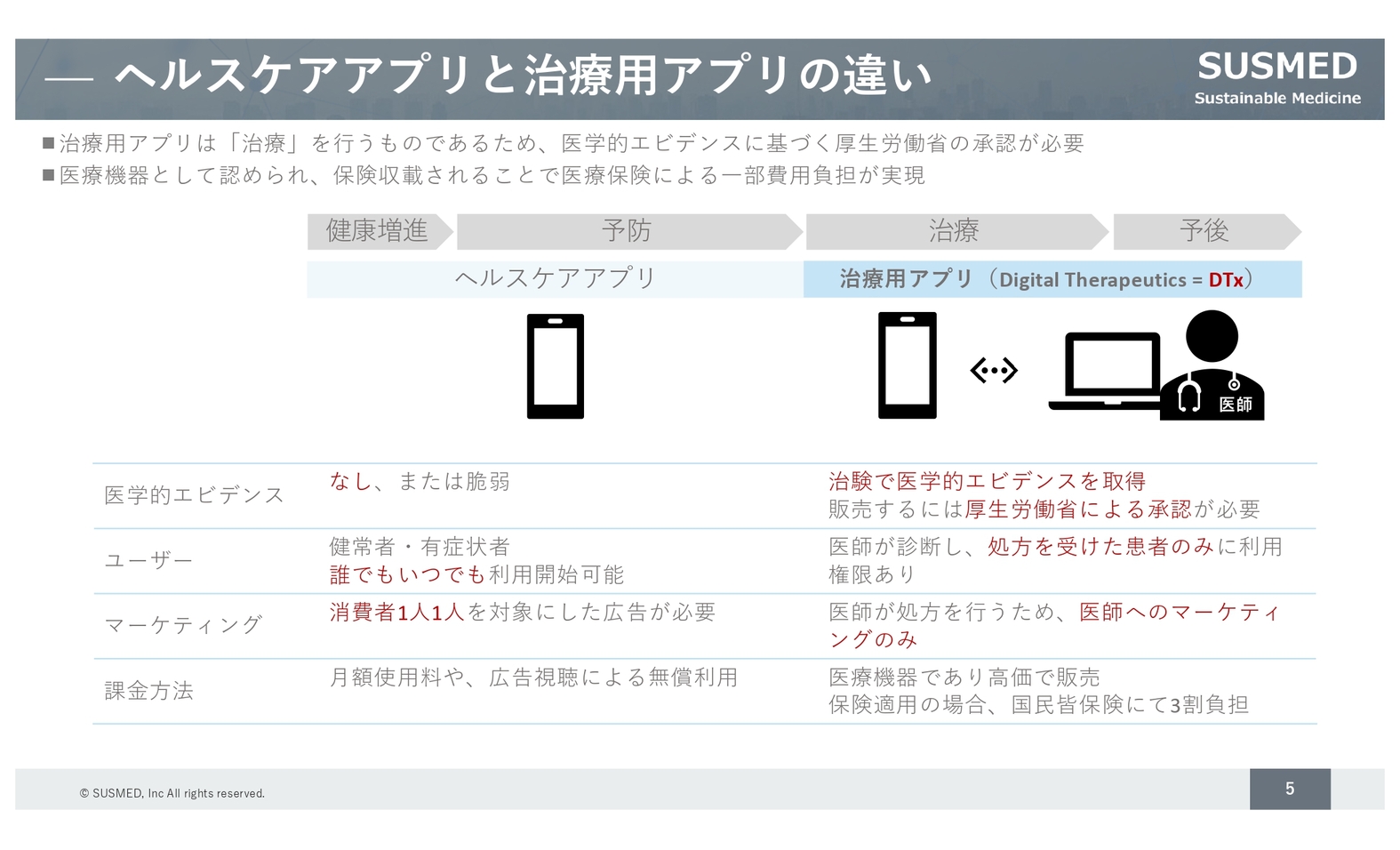
世の中にあふれているヘルスケアアプリとの大きな違いについてご説明します。現在のヘルスケアアプリはあくまで健康増進が目的のため、血圧の記録や歩数の記録等、健康増進のために使用されます。したがって、「治療」を謳うことはできません。
一方で、弊社の治療用アプリは医療機器に該当するため、治療を謳うことができます。そのためには治験を実施し、その治験結果をもとに厚生労働省の承認を得なくてはなりません。また、ご存じのように日本には国民皆保険制度がありますので、医療機器としての承認を得ることで患者の自己負担額を3割に抑えることができる点も大きなポイントです。
このように、一般のコンシューマーではなく、医師の診断と処方を受けた患者が使うため、医師に対するマーケティングが重要になってきます。こちらについては、製薬企業と連携しながら販売網を築いています。
開発パイプライン①(2023年8月10日現在)
開発中のパイプラインについてです。不眠障害治療用アプリはすでに治験結果をもとに承認を受けており、今は保険についての議論や、販売開始に向けた塩野義製薬との準備を進めている状況です。
がん患者向けアプリの「SMD401」と「SMD402」については、探索的試験やその次のステップに向けた準備をしています。また、慢性腎臓病患者向けのアプリ「SMD201」でも探索的試験が始まっており、「SMD402」と「SMD201」はともに前期の重点項目となっていましたが、両方とも被験者登録が完了しています。
その他にも、遷延性悲嘆障害やオピオイド誘発性便秘症のアプリを開発中です。また、耳鳴治療用アプリの「SMD403」は、杏林製薬と共同開発しています。乳がん切除後疼痛症候群のアプリは、名古屋市立大学の先生方と開発を進めています。
開発パイプライン②(2023年8月10日現在)
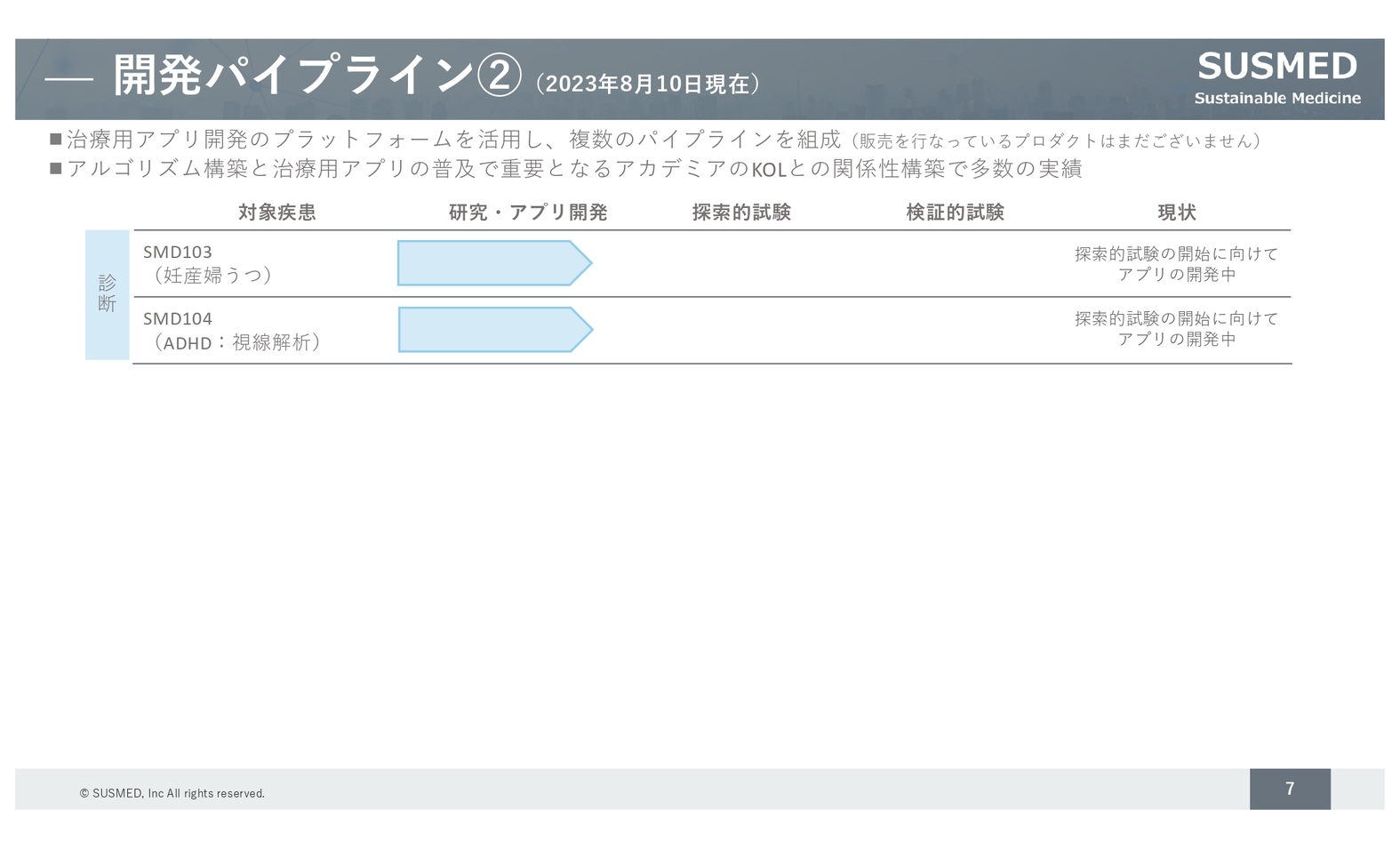
診断用については、妊産婦うつに対するアプリや、ADHDの患者の視線解析プログラムに関するアプリの開発も進めています。
現在は、8点の治療用アプリに加え、2点の診断用アプリを開発しています。
汎⽤臨床試験システム:SUSMED SourceDataSync
DTxプラットフォーム事業についてです。汎用臨床試験システム「SUSMED SourceDataSync」は、治療用アプリの開発ノウハウを集約し、スマートフォン経由でデータを集めることができます。さらに、弊社が特許を取得しているブロックチェーン技術を実装することにより、治験のレギュレーションをシステムでクリアする仕組みです。
これにより、治験で求められる臨床試験データのモニタリングに費やされる工数と費用を大幅に削減することができます。
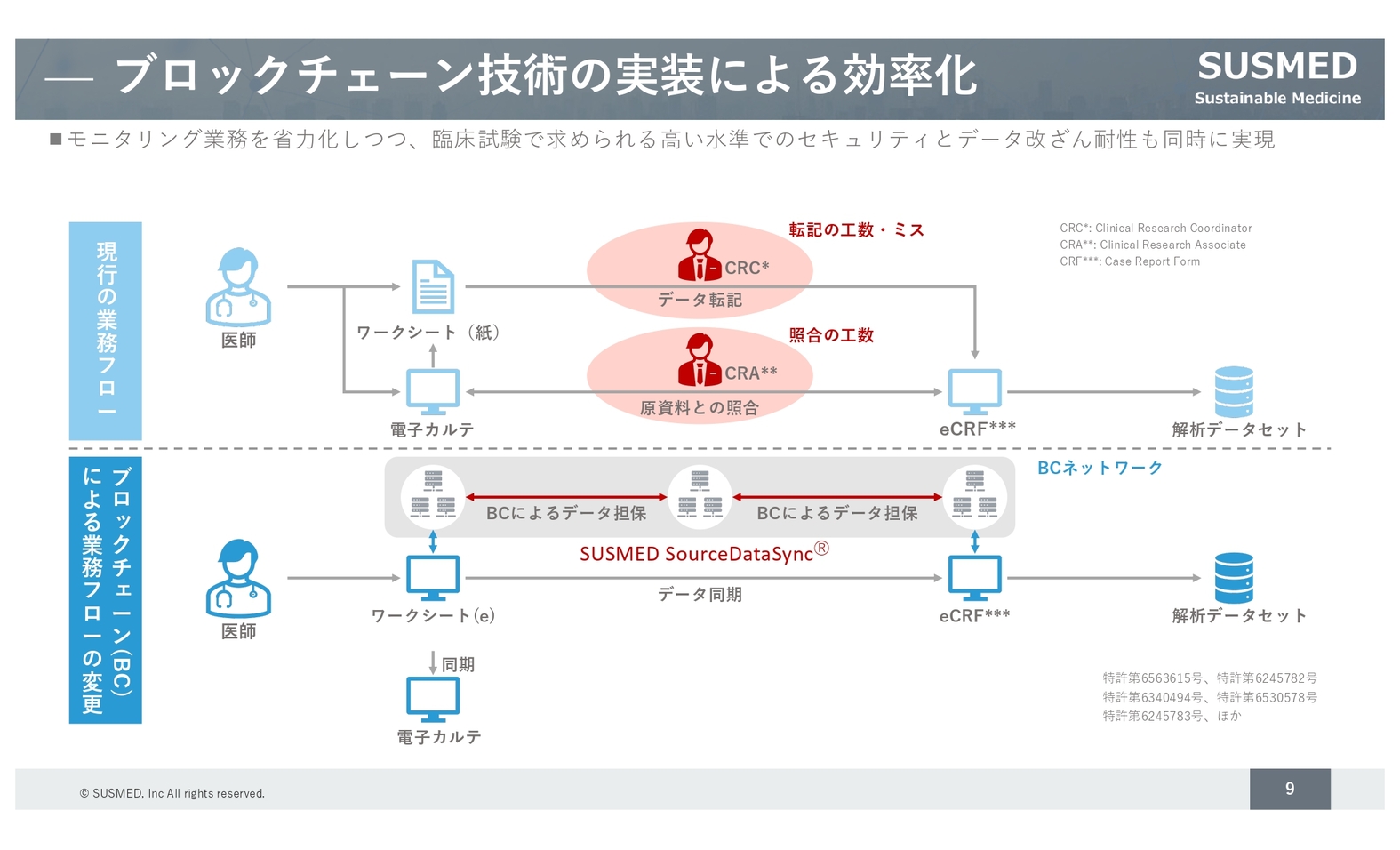
ブロックチェーン技術の実装による効率化
スライドには、ブロックチェーンの技術により、どのように治験が効率化されるかを示しています。治験業務では、医師が電子カルテに入力したデータをCRC(治験コーディネーター)が転記し、「eCRF」という症例報告書を作成します。この症例報告書のデータの信頼性を担保するため、GCP省令というレギュレーションが課されています。
データの信頼性を担保するために、これまでは、CRO企業から派遣されたCRAという職種の方が医療機関を訪問し、医療機関の電子カルテ情報である原資料との照合作業を目で行っていましたが、非常に労働集約的でした。
それに対して、弊社が特許を持つブロックチェーン技術を臨床試験に用いる仕組みを使うと、医療機関の原資料をブロックチェーン経由で「eCRF」につなげることができます。
これによってデータの転記が不要になるとともに、ブロックチェーンにはデータ改ざんを防ぐことができる特性があるため、原資料との照合作業をしなくてもデータの信頼性を担保することが可能になりました。この取り組みについては、厚生労働省からも正式にGCP省令に合致しているという通知を出していただいています。
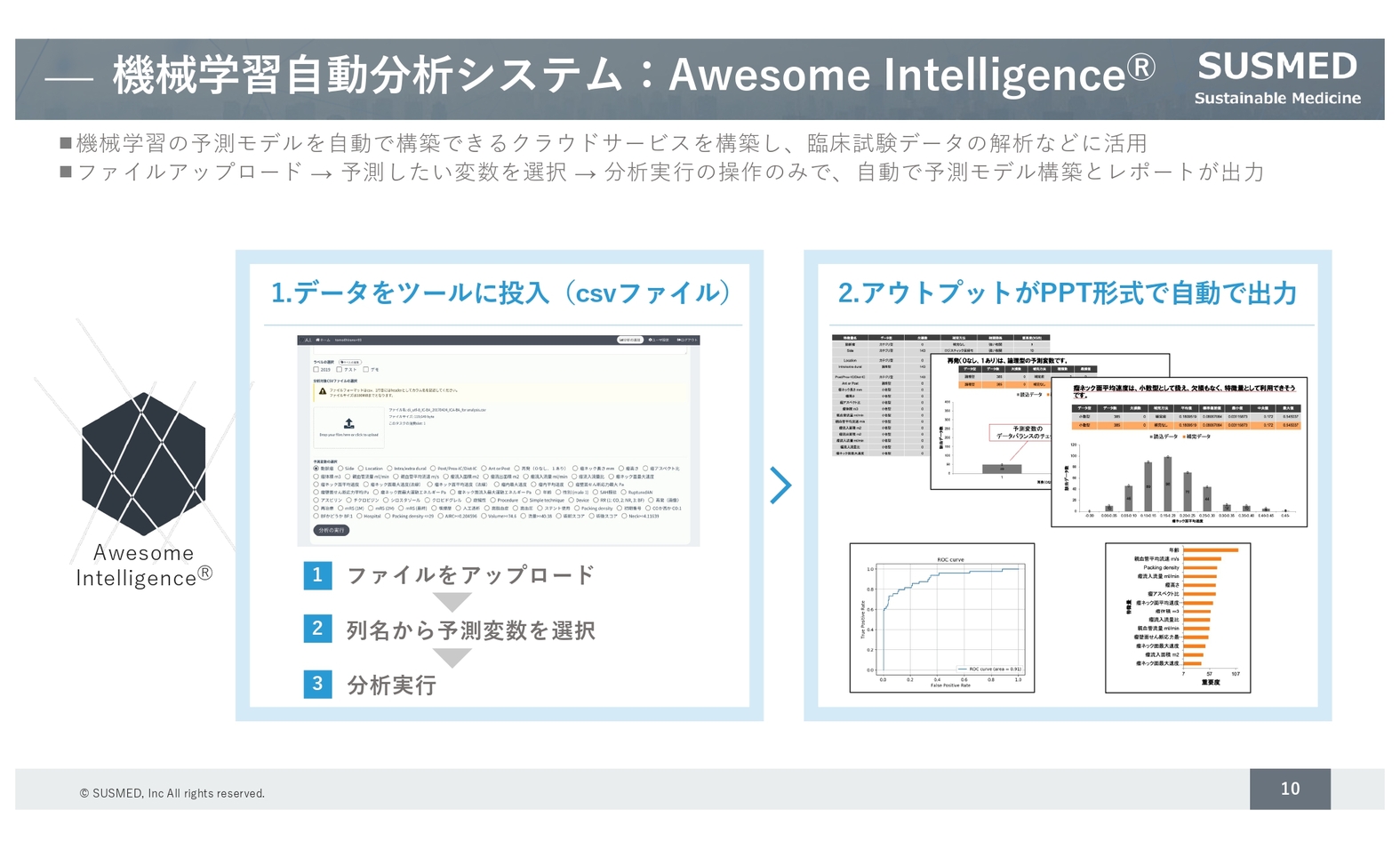
機械学習⾃動分析システム:Awesome Intelligence
機械学習⾃動分析システムについてです。今後、治療用アプリが世の中に出てくると、実際にアプリ経由でデータが集まってくることになるので、それを見越して準備をしているところです。
また、機械学習を効率よくできるクラウドサービスとして、いくつかの事業会社と共同で事業を展開しています。
2023年6月期 重点施策
前期に掲げていた4点の重点施策についてご説明します。1点目は、不眠障害治療用アプリの製造販売承認取得です。
2点目は、後続のパイプラインの開発進捗で、がん患者向けACPアプリ「SMD402」や、腎臓病患者向けアプリ「SMD201」の被験者登録の完了を目標に掲げていました。
3点目は、DTxプラットフォームの事業において、企業治験でのブロックチェーンを実装した臨床試験システムの稼働開始です。
4点目は、ブロックチェーン技術を応用領域であるレジストリなどにまで拡大させることです。
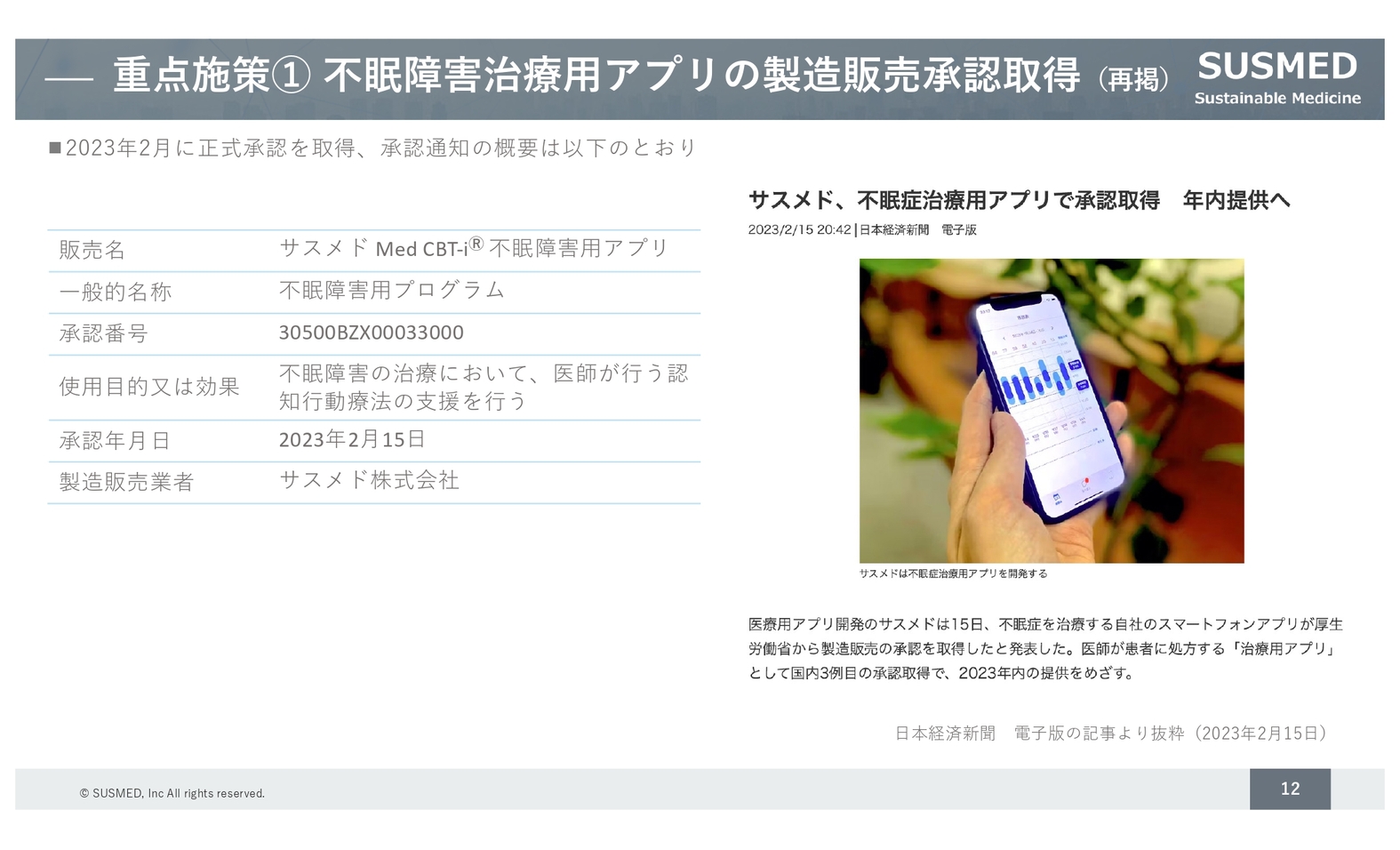
重点施策① 不眠障害治療⽤アプリの製造販売承認取得(再掲)
1点目の不眠障害治療用アプリについての進捗です。今年2月15日、厚生労働省から正式に承認を取得しました。同時に、パートナーである塩野義製薬からマイルストーンでの4億円を受領しています。
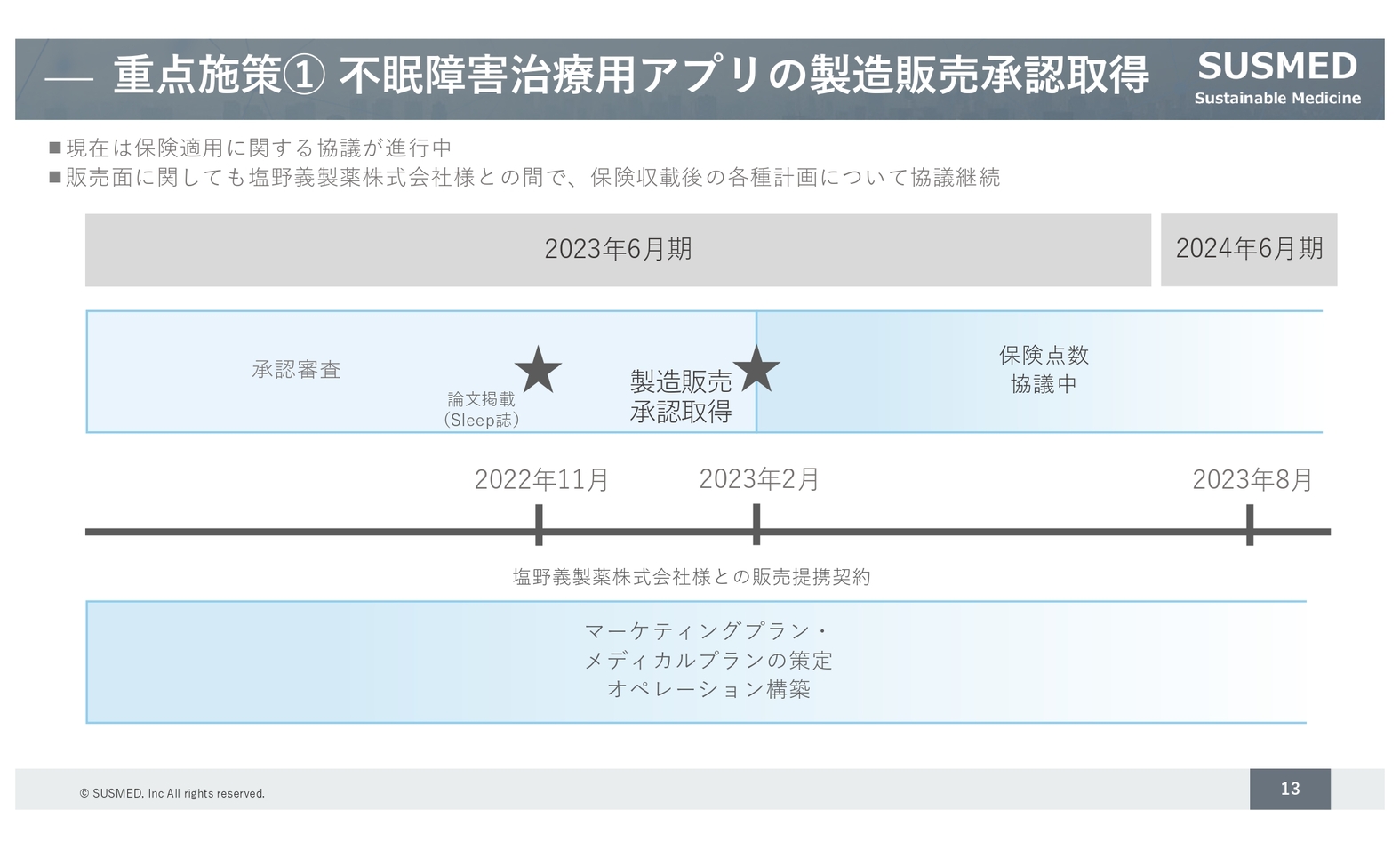
重点施策① 不眠障害治療⽤アプリの製造販売承認取得
現在は、厚生労働省の方々と保険適用についての議論を進めています。同時に販売の準備を進めており、塩野義製薬とマーケティングプランやオペレーションの構築を行っています。保険点数がつき次第、全国の患者に届ける準備を進めています。
重点施策② SMD402の臨床試験の進捗(再掲)
2点目のパイプラインについての進捗です。「SMD402」は「ACP(Advance Care Planning)」という、進行がん患者に対する治療用アプリです。現在は臨床試験を実施しておりますが、厚生労働省のサポートを受けながら進めてきました。
被験者登録がすでに完了していますので、観察期間が終わり次第、データを固定し臨床試験結果を解析する予定です。このアプリには、患者の不安抑うつ症状の改善や、死亡直前での抗がん剤使用といった不適切な治療を取りやめる効果があります。
重点施策② SMD201の臨床試験の進捗(再掲)
もう1つのパイプラインである慢性腎臓病患者向け治療用アプリ「SMD201」は、今まさに臨床試験を実施しているところで、被験者登録を完了させるという目標は達成できました。
慢性腎臓病患者とは、いわゆる腎不全による透析予備軍の方々のことで、日本国内で約1,300万人患者がいます。このアプリは東北大学や学会の先生方にご協力いただきながら開発しています。
慢性腎臓病患者向け治療用アプリは腎機能の悪化を抑制できるため、患者が透析に移行するのを防ぐ効果が期待されます。こちらについても、被験者の観察期間が終わり次第、データを固定し、解析していきます。
2023年6⽉期 重点施策の達成状況
3点目の重点施策では、すでに企業治験での採用実績が2件出ています。現在は、その採用実績をもとに、複数の企業への提案を加速させている状況です。
4点目のブロックチェーン技術の治験領域以外への応用では、レジストリでの活用に向け、複数の企業と協議を進めています。
その他
そのほかのトピックです。取締役の指名や報酬に関する事項の諮問機関として、ガバナンス委員会を設置しました。
また、創業以来、弊社に貢献してきた取締役の市川が退任しました。市川は臨床開発を管掌していましたが、私が臨床開発機能については引き継いでおり、全体として問題なく運営しています。
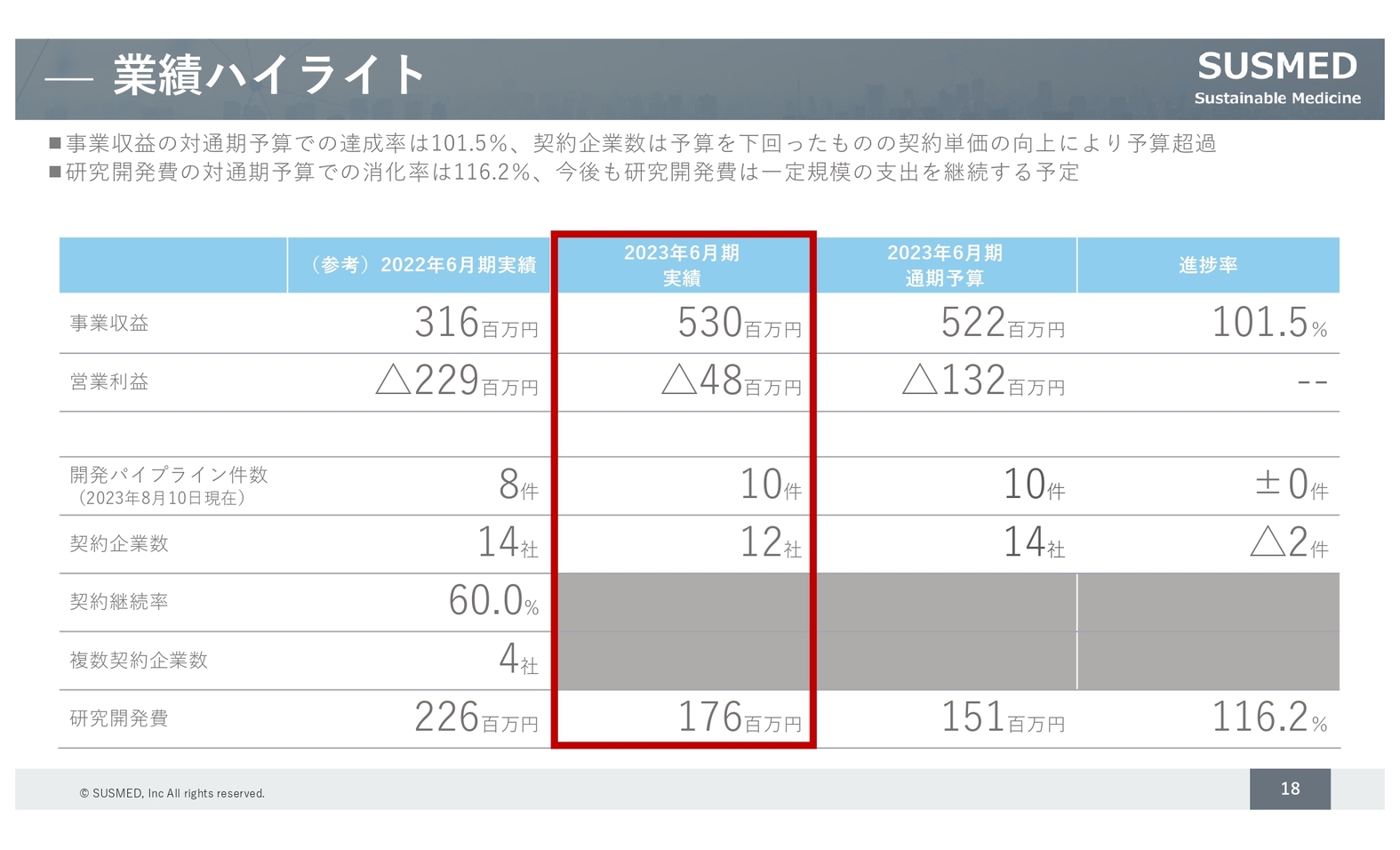
業績ハイライト
業績ハイライトです。事業収益は、通期予算5億2,200万円に対し、5億3,000万円で着地しました。前々期の3億1,600万円から着実に増えています。また、研究開発費については、今後も一定規模の支出を継続していく予定です。
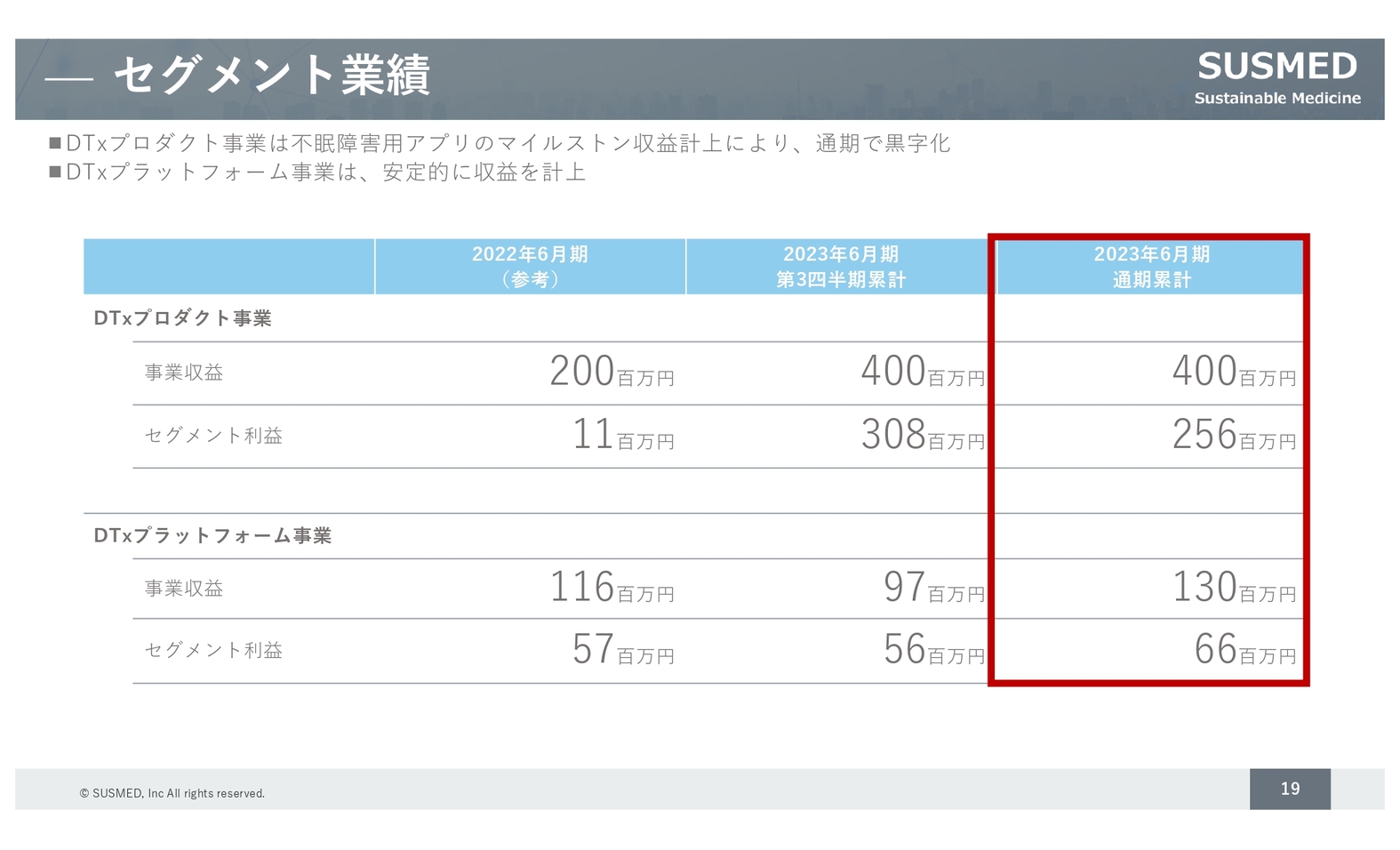
セグメント業績
セグメントごとの業績です。DTxプロダクト事業については、先ほどもお伝えしたように、不眠障害用治療用アプリが承認を取得しマイルストーンを達成したため、塩野義製薬から4億円を受領しました。
今後も不眠障害治療用アプリの進捗に応じてマイルストーンが発生するかたちとなっており、41億円が残っている状況です。さらに実際の販売開始後は、ロイヤリティがしっかりと入ってくる予定です。
また、DTxプラットフォーム事業についても、安定的に収益を計上できています。売上以上に、ブロックチェーンを使った世界初の治験事例を出すことができたため、こちらをレバーにしてさらに拡大していけたらと考えています。
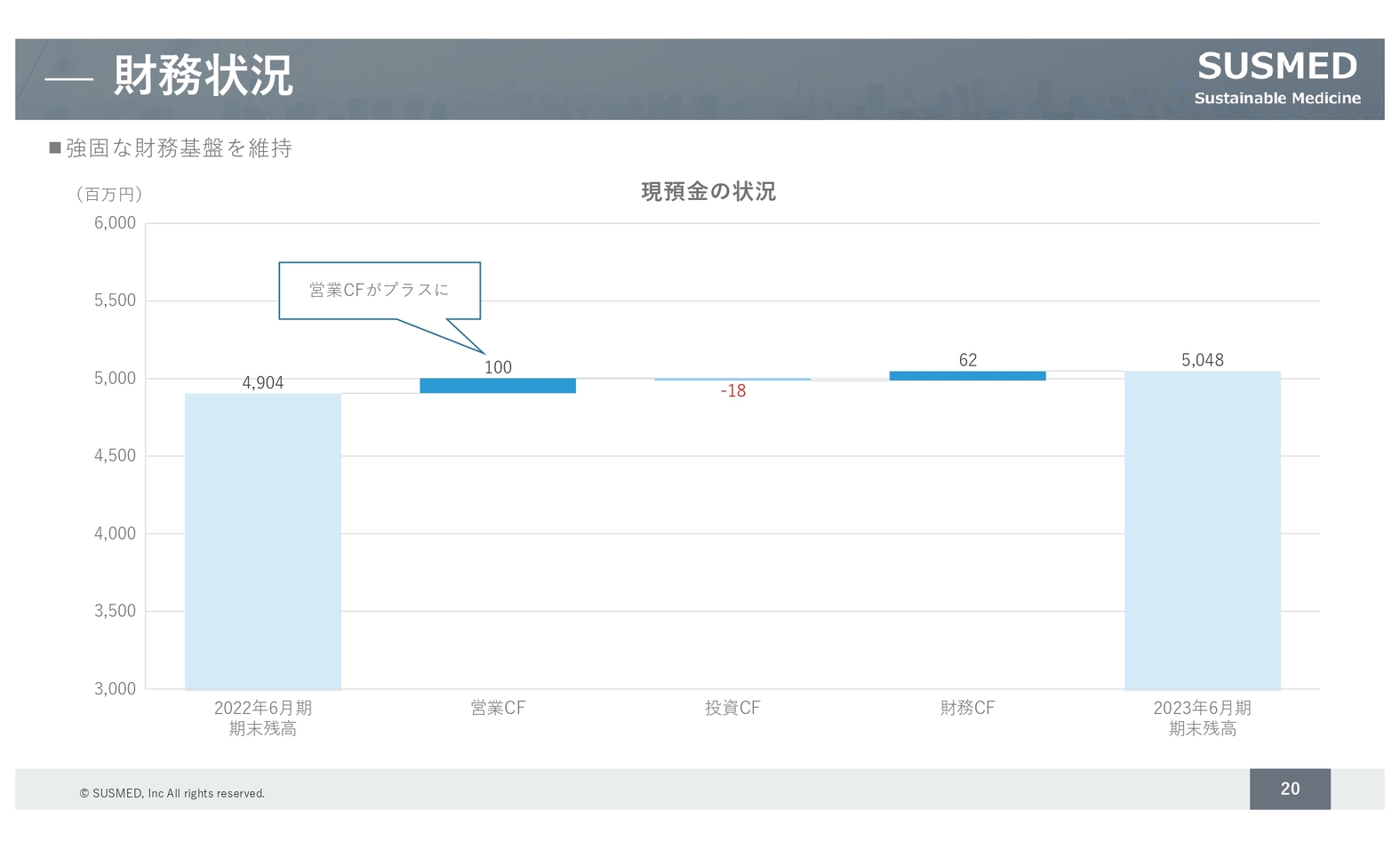
財務状況
財務状況は、今期は、営業キャッシュフローがプラスになった点が1つの大きなポイントだと思います。期末残高については前々期末の49億円に対し、50億円と増加しています。
2024年6⽉期 重点施策
業績予想については、現在、不眠障害治療用アプリの保険点数を厚生労働省の方々と議論しているところなので、確定次第、開示させていただく予定です。現時点では申し訳ありませんが、非開示とさせていただきます。
今期の重点政策についてご説明します。
1点目は、不眠障害治療⽤アプリの販売開始です。それに紐づいてマイルストーンやロイヤリティが発生し、本格的な収益の計上が今期から始まります。
2点目の後続のパイプラインについては、研究開発をしっかりと前に進めていく予定です。実際に、前期と比べてパイプラインが増えていますので、探索的試験を実施したものについては、当局と議論しながら検証的試験の準備を進めていきます。
臨床研究を開始する「SMD403」や、これから探索的試験を開始する「SMD105」についても、今期中に開始したいと考えています。
3点目のDTxプラットフォーム事業については、ブロックチェーンを活用したフェーズⅢの治験がすでに複数走っています。その実績をもとに新規案件を獲得していくことが、重点施策になっています。
4点目のブロックチェーン技術の治験以外への応用については、前期から重点施策にあげていましたが、今期はレジストリの構築をしっかりと開始したいと考えています。私からのご説明は以上です。
質疑応答:不眠障害治療⽤アプリの契約や他アプリの引き合いについて
質問者:不眠障害治療の分野に興味を持っている日本のファーマはたくさんあると思います。中でも塩野義製薬は、次の成長ドライバーの1つとして考えているとのお話でした。
今後は薬価収載される製品が増えていくと思いますが、塩野義製薬とはどのような契約になっていますか? また、塩野義製薬はこの分野(不眠障害)以外にも興味を持っているのかどうか教えてください。
上野:塩野義製薬との契約内容ですが、秘密保持義務があるため詳細は開示できません。定量的な部分については、マイルストーンやロイヤリティの発生ベースでご報告するかたちになると思います。
弊社としては不眠障害治療⽤アプリの売上を上げ、収益を最大化していく考えです。今回もあくまで販売提携の契約であり、承認取得まで私どもで完遂しています。そのため、初期に導出する場合の小さな料率でのロイヤリティの構図とはまったく違うことはご理解いただければと思います。
塩野義製薬の興味関心について当社から言及することは差し控えますが、他のパイプラインとして、耳鳴のアプリを杏林製薬と共同開発していたり、現在開示しているその他の治療用アプリについても、ご関心をお持ちいただいている製薬企業があります。
ただし、弊社はパイプラインの価値を最大化させることをメインに考えているため、どの段階でどの企業とパートナリングするかについては、プロダクトごとに戦略を構築することになります。
共同開発については、弊社が開発プラットフォームを用意していることもありますので、興味関心をお持ちいただける製薬企業であればディスカッションをさせていただく方針です。
質問者:今回業績は未発表ですが、前期でのマイルストーンの残りが41億円とのことでした。医療機器のため償還というかたちになるかもしれませんが、薬価収載が決まった段階でいただけるものはかなり大きくなると考えてよいでしょうか?
上野:ロイヤリティの部分については、点数が決まってから実際の販売計画を立てることになります。これは塩野義製薬との議論が必要になるため、単価と想定している処方数を掛け合わせたものに合意した上で、開示することになります。
マイルストーンについても事前にはお伝えできませんが、通常は販売後も販売のマイルストーンなどが組まれるため、イメージとしては今期に41億円すべてが計上されるのではなく、販売開始後もマイルストーンとして踏んでいくイメージです。
質問者:41億円すべてではなくても、かなりの額が入ってそれなりの利益が出るイメージでよろしいでしょうか?
上野:量的なところについての回答は控えますが、弊社はもともと販売前の段階で多くのマイルストーンを踏む予定ではありません。総額47億円のマイルストーンのうち残り41億円あるということは、逆に言えば私ども自身で承認までやりきれると考えたため、前で取らずに後ろで取ることで最大化できると判断したことの表れです。
質問者:処方人数に応じてマイルストーンがクリアされるというイメージでしょうか?
上野:おっしゃるとおりです。販売におけるマイルストーンは、通常の場合、処方数ごとに設定されると思います。
質疑応答:慢性腎臓病患者向け治療⽤アプリ「SMD201」について
質問者:「SMD201」を提供する慢性腎臓病は非常にマーケットが大きいということで、御社の試算でも660億円となっています。慢性腎炎のダイアライザを扱うニプロやポンプ会社の日機装、またはホルモン剤を手掛けている会社など多数ありますが、御社の(提携の)ターゲットとなるのはどのような会社でしょうか?
上野:ニプロのダイアライザなどはすでに人工透析を行う方々に使われるもので、私どもの慢性腎臓病治療用アプリはその前段階を想定しています。現在、日本国内に人工透析を受けている方は30数万人いらっしゃいますが、人工透析の予備軍である慢性腎臓病の方は約1,300万人おり、非常に大きなマーケットになっています。このアプリは、そのような方々を対象にしているイメージです。
質問者:人工透析を行っているメーカーよりも、さらに幅広いターゲットを対象としているイメージでしょうか?
上野:おっしゃるとおり、人工透析の前段階の方々をターゲットとしています。マーケットが大きいということで、現在、慢性腎臓病治療薬の開発に注力されている製薬会社は内資・外資を含め多くいらっしゃいます。
質疑応答:不眠障害治療⽤アプリの浸透・拡大について
質問者:不眠障害治療⽤アプリ上市後のマーケティングあるいは流通方法や、処方医への使い方のガイダンスなど、速やかに処方を広げるための施策について、お話しいただける範囲でお聞かせください。
上野:まず不眠症の治療において、第1選択で推奨されているのは認知行動療法であるとガイドラインに位置づけられています。さらに海外、例えばイギリスでは、認知行動療法をアプリで行うことが、睡眠薬よりも推奨されると国のガイドラインにも明示されています。
そのような位置づけの中で、私どもの不眠障害治療⽤アプリは国内で初めて開発されたものであり、ファーストインクラス(画期的医薬品)になります。
臨床現場において睡眠薬よりも認知行動療法や非薬物療法が推奨されることついては、臨床医の先生方もご認識されています。塩野義製薬のMRが臨床医の先生方にそういったメッセージとしてお伝えしていくことが、実際の販売計画になります。
質問者:その浸透イメージについて、初年度でどれだけの医療機関に導入してもらうか、あるいは何人の患者に使用するかなど、今の段階でつかめている部分はありますか?
上野:不眠障害治療用アプリのSAM(Serviceable Available Market=ある事業が獲得しうる最大の市場規模)については、スライドに記載しているとおりです。
初年度でどのくらい浸透できるかについては、通常医薬品のマーケティングでは販売開始から5年ほどかけてピークセールスに持っていくこともあり、塩野義製薬も同様のイメージを持っていると考えています。
質疑応答:企業治験プロジェクトの売上規模について
質問者:臨床試験システムについてうかがいます。今決まっている企業治験は2件だと思いますが、こちらのプロジェクト当たりの売上規模はどのように決まるのでしょうか?
また、これから獲得していくものについてどのようなモダリティであるか、対象患者が多いか少ないかなど、製薬会社やプロダクトのプロファイルはどのように進めるイメージになりますか?
上野:こちらについては、治験のプロトコルに依存するというのが実状です。CRO企業の売上の半分ほどを占めるモニタリング業務の代替として、システムを活用していくイメージです。実際には、症例数や観察期間などの治験規模によって価格は増減すると考えています。
一方で、CRO企業がCRAという職種の方を1人につき月200万円で、規模によっては10人ほどを抱えて複数年にわたり継続するような治験があります。その場合、弊社のシステムを使うことによって半分の人員で回せるようになると、削減できた部分から収益をいただくことができます。このように、完全に治験の規模に依存しているのが実状です。
質疑応答:新年度の研究開発費について
質問者:新年度の研究開発費について、DTxプロダクト事業とDTxプラットフォーム事業にわけて教えてください。
上野:研究開発費の増減としては、パイプライン開発の治験コストのインパクトが一番大きなところになります。
開発中のパイプラインでそれなりの規模の治験を実施する場合、検証的試験に入るタイミングで大きな研究開発費が発生します。PMDA(Pharmaceuticals and Medical Devices Agency)ともプロトコルの協議はしますが、先方の意向もあります。
また、弊社の臨床試験システムは製薬企業に使ってもらうだけではなく、弊社自身が治験をする際にも使う方針です。このような工夫により、製薬企業であれば何十億円とかかるところを、かなり圧縮した状態で実施できるとは思っています。
基本的には、それぞれのパイプラインが検証的試験に入るタイミングで、億単位のコストがかかってくるイメージです。
質問者:DTxプラットフォーム事業には、それほどコストはかからないのでしょうか?
上野:おっしゃるとおりです。DTxプラットフォーム事業についてはベースとなるシステムがあるため、追加のアップデートなどに研究開発費がかかる程度です。
質疑応答:不眠障害治療⽤アプリの発売開始予定について
質問者:不眠障害治療⽤アプリの保険収載のタイミングについてうかがいます。2月に承認されてから6ヶ月が経ちますが、発売開始は今月か来月ぐらいを想定してよろしいでしょうか? もしくは、ご説明の中で「交渉中」という単語がありましたため、下期に偏ると想定したほうがよいのでしょうか? タイミングについての示唆をお願いします。
上野:保険収載のタイミングは厚生労働省のタイムラインによるため、私どもでコントロールできないことが前提となっています。
弊社としても遅くとも年内には発売開始をしたいと考えており、厚生労働省も間に合わせてくれるのではないかと考えています。ただし私どもがコントロールしたり、時期を明言したりできないことをご理解いただけますと幸いです。
質問者:診療機器の価格交渉がどのように行われるのかを正確には把握していませんが、薬の場合、御社から「このような価格とロジックでお願いします」と提案して、当局に承認されれば話が進むと思います。今はボールが当局側にあり、御社は返答を待っている状況と理解してよいでしょうか? それとも、まだやり取りしている状況でしょうか?
上野:基本的には待っている状況です。
質疑応答:不眠障害治療用アプリの立ち上がりのイメージについて
質問者:不眠障害治療用アプリの立ち上がりのイメージを再度教えていただきたいです。海外だと認知行動療法が第1選択肢になっていますが、日本だとそれに相当するものがなく、対面でもなかなか診療ができていません。
その状況下では、鋭く立ち上がってもよいのではないかと思います。一方で、なかなかドクターがこのようなアプリを処方しない、または処方しにくいというボトルネックもあると思います。最初はどのくらいの角度で立ち上がっていくかなど、臨床医としてのヒントがあれば教えていただけないでしょうか?
上野:私たちも、まさに臨床現場でのオペレーションの精査や整備を進めています。例えばITに詳しくない医師でも、ハードルなく処方できるようなオペレーションを塩野義製薬と構築しており、医師の対応がボトルネックにならないように準備を進めています。
その中で、実際にどのような時間軸で立ち上がるのかについては、医師側に処方することの臨床的な意義がきちんとあることが非常に重要だと思います。実際に、睡眠薬の過剰処方についての議論では、約98パーセントの臨床医が「睡眠薬はよくないと思いながら処方している」と回答しています。
その点を解決できるソリューションとして、きちんと医師側に認識されれば、使っていただけると期待しています。
一方で、通常の医薬品のみならず、ファーストインクラスのものであっても、発売から急峻に立ち上がることはなく、5年ぐらいかけて徐々に浸透していくと聞いていますので、現時点ではそのようにイメージしています。
質疑応答:「SMD402」と「SMD201」の進捗について
質問者:「SMD402」と「SMD201」についてです。今期に検証試験開始予定とありますが、すでに御社の中では探索的試験が良い結果であることがわかっているため、検証的試験を始めると記載しているのでしょうか?
我々に対しては、結果も含め、しかるべきタイミングで今期年末から来年にかけて開示されますか? 現在の進捗について、もう少し教えてください。
上野:「SMD402」と「SMD201」の結果については、まだ弊社でも確認しておらず、これからという状況です。探索的試験後の検証的試験については、当然ながら探索的試験の結果をもとに規制当局と相談したり、プロトコルの議論をしたりする必要があります。
そのため、開始ではなく「準備に着手する」という意味合いで記載しています。
質問者:そうしますと、探索的試験結果の開示のタイミングは、今年の年末から来年にかけてというイメージで間違っていないでしょうか?
上野:論文投稿後の査読に時間がかかることや、学会発表などのスケジュール調整が入ると思います。そのため、イメージとしては来年中となります。
質問者:順番としては、論文が出た後に検証的試験が始まると捉えてよろしいですか?
上野:検証的試験を始めるとしたら、おそらくそうなると思います。当然ながら、PMDAとの議論にも一定の時間がかかります。
質疑応答:「SMD402」と「SMD201」の研究開発費について
質問者:「ACP」用の「SMD402」と慢性腎臓病治療用の「SMD201」の検証的試験は、来年以降にスタートということであれば、今期の研究開発費はそこまで大きくならないというイメージでしょうか?
今期はまだガイダンスが発表できない状況で、売上がどのようになるかはわからないと思います。ただし、来期に2本一気にスタートすれば、10億円を超えるかもしれないという印象です。
また、不眠障害治療用アプリの立ち上げスピードによっては、先行投資がけっこうかかるかもしれません。来年、不眠障害治療用アプリの売上がある程度立てば、検証的試験の費用もカバーできるのではないかと思っていますが、そのあたりのイメージについて教えていただけますか?
上野:ご指摘のとおり、収益もコストも「SMD402」と「SMD201」の検証的試験のタイミング次第になると思います。先ほどお話ししたように、今年は解析結果について実際に確認し、論文を書いたり、その結果をもとに規制当局とプロトコルについて相談したりする段階に入ると思います。
したがって、先ほどもお答えしたとおり、今期の早い段階で検証的試験に入ることはなく、来期が本格的な検証的試験の実施時期だと考えています。
ご質問のとおり、検証的試験までに不眠障害治療用アプリがどのぐらい立ち上がっているのか、また弊社のブロックチェーン技術をフル活用して、コストを下げながら治験のプロトコルおよび治験自体をどこまで効率的にできるかについても、最大限努力します。研究開発費については、これらの状況との兼ね合いになると考えています。
質問者:不眠障害治療用アプリの被験者数は、156名と少なく済んでいます。「SMD402」と「SMD201」の検証的試験の具体的な被験者数は、これからのPMDAとのお話次第だと思いますが、156名よりは大きくなる可能性もあるのでしょうか?
上野:可能性はあると思います。製薬メーカーの試験では通常、検証的試験が156名程度で済むことはまずありません。ですので、不眠障害治療用アプリの検証的試験が非常に効率良くできたことは事実だと思います。
そのため、156名よりは多くなるとは思いますが、天井がないのも困りますので、私どもとしてはできるだけ症例数をコンパクトにしたいと考えています。
また、治験は期間も重要です。例えば、がんの治験では非常に長い治験期間が設定されます。不眠障害治療用アプリの場合は、治験期間が1患者あたり2ヶ月と比較的コンパクトに済んでいますので、期間との兼ね合いもあると思います。
したがって、「SMD402」と「SMD201」については、それなりの治験コストがかかると認識しています。
質疑応答:貸借対照表のソフトウェアという項目について
質問者:貸借対照表の無形固定資産のところに「ソフトウェア」という項目があります。今までは「無形固定資産」とだけ書いてあり、中身がよくわかりませんでしたが、ソフトウェア開発アプリについては即費用計上する会計方針だったと思います。
このソフトウェアとは何に関連するものなのでしょうか? また、今後もそのような開発コストを資産として計上し、償却するケースがあるかどうかについても教えてください。
小原隆幸氏(以下、小原):こちらは、アキュリスファーマの治験で使用しているソフトウェアの構築費用を無形資産として計上しています。今後、「SUSMED SourceDataSync」のクライアントが増えると、それぞれの案件で構築したシステムが無形資産に計上される可能性はあります。
質問者:では、アプリに関しては今までどおりという認識でよろしいでしょうか?
小原:おっしゃるとおり、治療用アプリに関しては今までどおり即費用計上です。
質疑応答:2024年6月期の予算と適正使用ガイドラインについて
質問者:2024年6月期の予算が示されていないことは理解していますが、今までの質問の回答からすると、タイミングとしては、不眠障害治療用アプリの保険点数(薬価)が保険収載された後に開示されるという理解でよろしいですか?
上野:そのとおりです。現時点では保険点数がはっきりしていないため、今期の業績予想は出していません。業績予想が出せるようになり次第、開示させていただく予定です。
質問者:そのような意味では、例えば保険収載が8月に完了すれば、それ以降の決算発表でのご説明になるということでしょうか?
上野:おっしゃるとおりです。
質疑応答:不眠障害治療用アプリの適正使用ガイドラインが出るタイミングについて
質問者:少しニッチなところかもしれませんが、不眠障害治療用アプリの適正使用ガイドラインが出てくる想定で見ています。そのタイミングについては保険収載のタイミングと同時と考えてよろしいでしょうか? それよりも前ということもあり得るのでしょうか?
上野:適正使用ガイドラインは、通常、保険点数のタイミングと同時に出てくると想定しています。
質疑応答:不眠症の薬剤投与への認識について
質問者:医療用アプリ自体は、すでにニコチン用や高血圧用のものが出ています。
先ほどのご説明では、専門医の約98パーセントが不眠症の患者に対して薬剤投与は良くないと思っているということでした。一般的には、そのような理解はそれほど進んでいないと思います。しかし、外部から見ると、専門医の方はこのアプリを相当認識しているのではないかと思いますが、専門医でもある上野社長はどのように理解されていますか?
上野:おっしゃるとおり、すでにニコチン用や高血圧用のアプリは市場に出ています。
一方で、一般の方だけではなく医師側も、おそらく医療現場では治療用アプリが広がっていないと認識していると私自身も思っていますし、意見としても聞いています。治療用アプリの普及のために非常に重要なことは、医師が処方を判断する際に、このアプリがどのように貢献するかだと思います。
既存の医薬品でよいのであれば、現状の薬を処方し続ける医師が多いと思います。現状の薬に問題がある、あるいはそもそも薬がない疾患に対して、問題解決の新しいツールとしてアプリが出てくると、医師の「処方する」という行動にもつながると思います。
実際、睡眠薬の過剰処方は以前から非常に問題になっており、国も睡眠薬の適正使用を啓蒙しています。
また、先ほどお話ししたように、海外では国のガイドラインで、特に不眠症の分野において睡眠薬よりもアプリが推奨されています。それだけ、不眠症分野において、睡眠薬の過剰処方を是正しなければいけないという意識のレベルが高いということです。
医師もみな良くないと思いつつ、患者に「飲み続けると良くないですよ」と言いながら睡眠薬を処方しているのが現状です。そのため、アプリそのものの認識というよりも、現状の不眠症治療法に満足しているかどうかが普及するかどうかの一番大きなポイントになると思っています。
質問者:それはやはり、御社や塩野義製薬が協力して、そのような啓蒙活動をある程度行わなければ、なかなか普及しないということですか?
上野:睡眠薬が問題であることは、約98パーセントの臨床医が認識しています。そして、不眠症の治療を睡眠薬ではなく認知行動療法が担えるということも、基本的にほぼすべての医師が認識しています。
ただし、認知行動療法をアプリで提供できるということについては、塩野義製薬のMRが広めていく必要があると思います。この部分だけの活動であれば、そこまでハードルは高くないと思います。
このアプリは、睡眠薬は良くないと思っている上に、患者から「睡眠薬を減らしたい」と言われながらも睡眠薬を処方せざるをえない現状に刺さるのではないかと期待しています。実際に、塩野義製薬にもそのようなアンメットメディカルニーズがあるプロダクトだと理解してもらえたからこそ、販売提携契約につながったのだと思っています。