2020年5月13日に行なわれた、エーザイ株式会社2020年3月期決算説明会の内容を書き起こしでお伝えします。
スピーカー:エーザイ株式会社 代表執行役CEO 内藤晴夫 氏
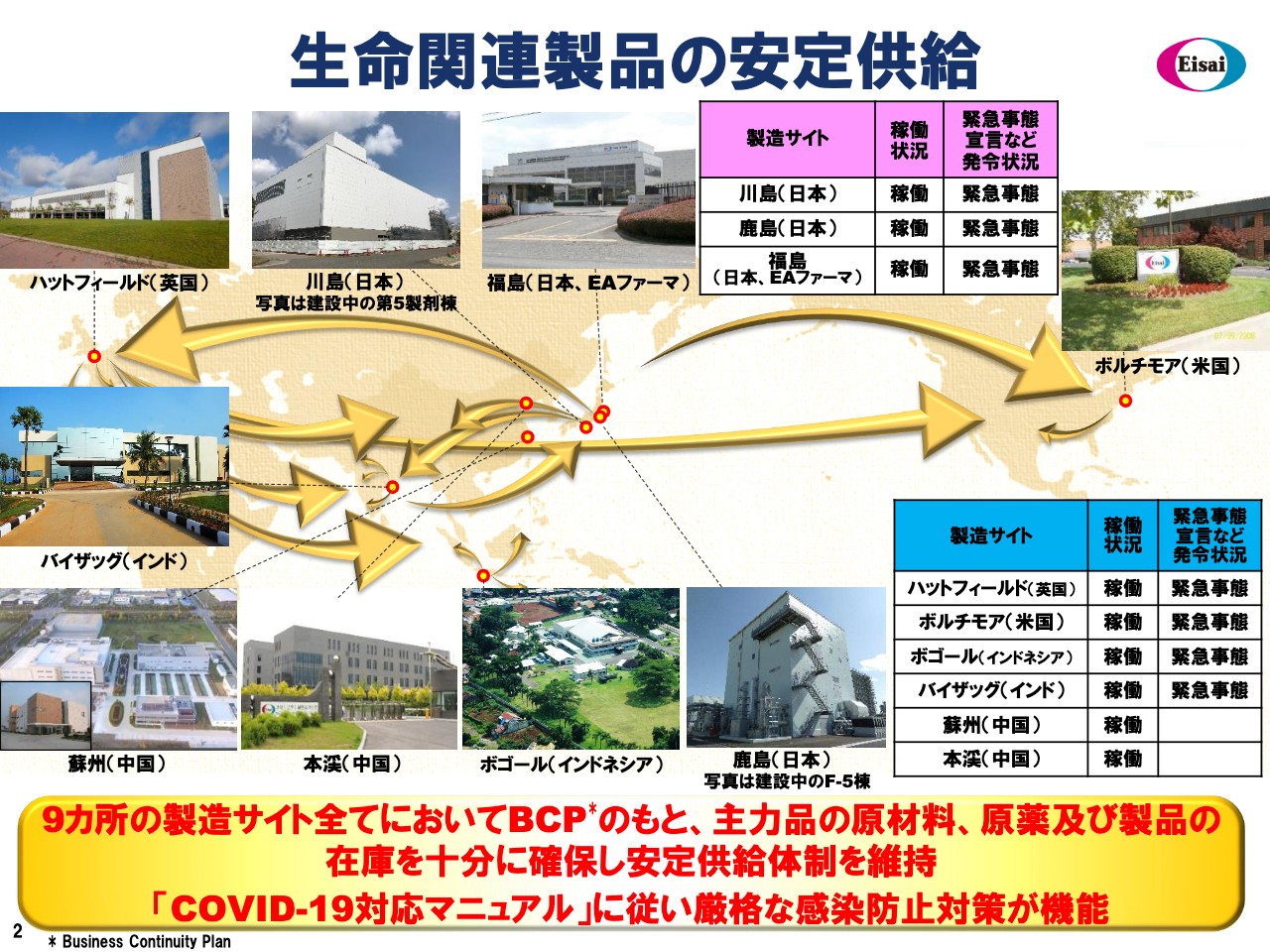
生命関連製品の安定供給
内藤晴夫:内藤でございます。2019年度の決算についてご報告します。現況のCOVID–19のパンデミック化です。私ども製薬企業も果たすべき数々の役目を担っていると考えていますが、そのなかでも非常に重要な部分が、スライドでお示ししているような自分たちの製品の安定供給だと思います。言うまでもなく、すべての医薬品は患者さまのクオリティ・オブ・ライフ、あるいは生命に直結する生命関連製品ですので、この途絶は許されないと考えています。
このスライドでは、私どもがグローバルに展開する9つの生産拠点の様子をお示ししています。それぞれの製造サイトが置かれている緊急事態宣言などの状況は異なりますが、現在9つすベての製造サイトで順調な稼働が行なわれています。安定供給がしっかりと実践されている状況です。この安定供給を保つには、十分な原材料、原薬、あるいは原薬の中間体、包装材料などを在庫として持ちながら生産活動を継続していく「Business Continuity Plan」が大変重要になってきます。現在、主力製品については平均で4ヶ月から5ヶ月を超える十分な最終製品の在庫を有している状況です。
もう1つ大事なことは、この現場で操業に従事し、社員のみなさまの安全を守ることです。社内で定めた「COVID–19対応マニュアル」に従い、厳格な感染防止対策を実施しながら安定供給に努めている状況です。
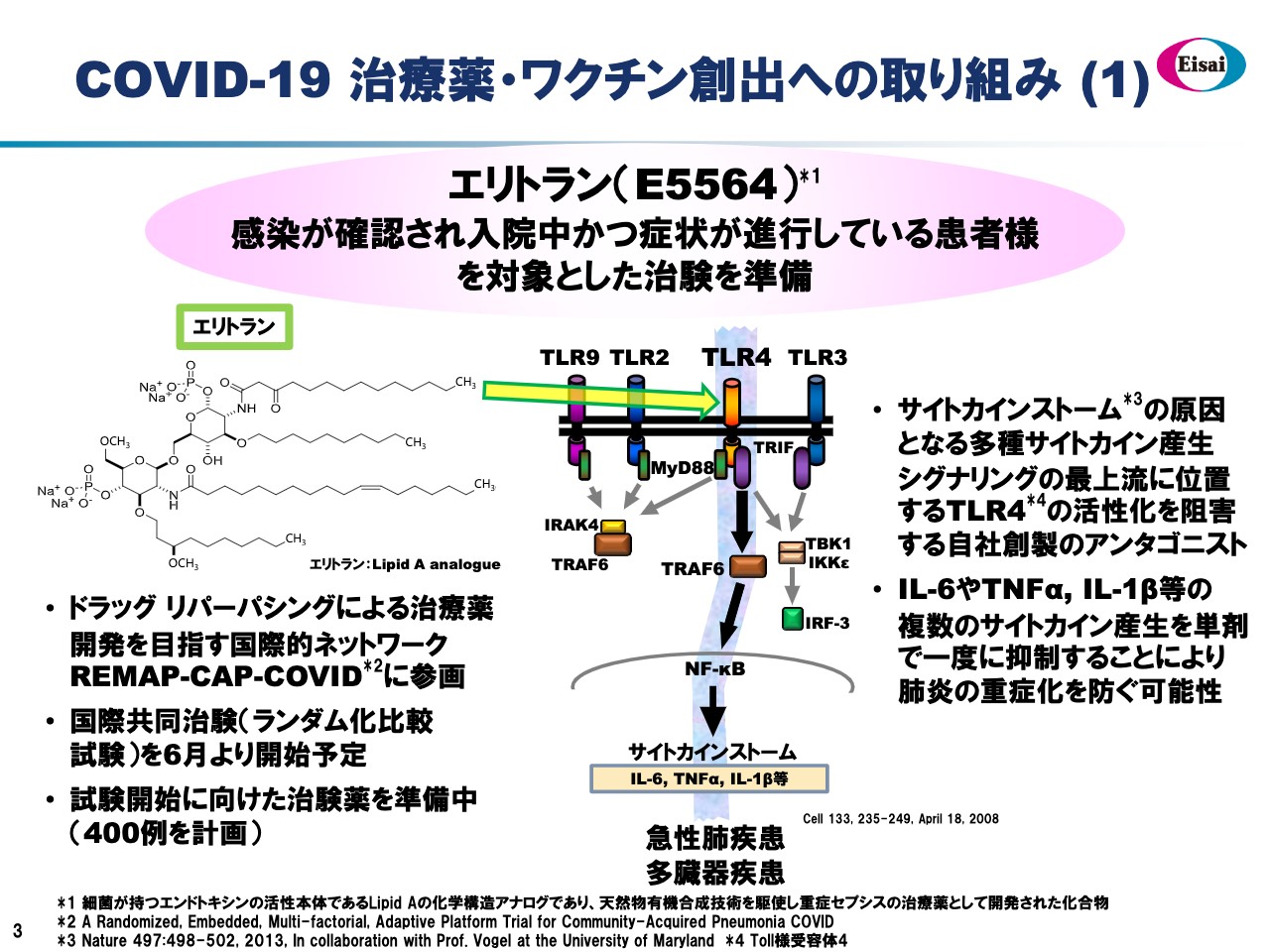
COVID–19 治療薬・ワクチン創出への取り組み(1)
もう1つの役割は、COVID–19に対する治療薬、あるいはワクチン創出への取り組みです。この観点から、本日はまず第一に「エリトラン」の可能性についてご報告したいと思います。「エリトラン」は、細菌が持つエンドトキシンの活性本体であるLipid Aの化学構造アナログです。当社のボストン研究所で非常に高度な天然物有機合成技術を駆使して合成しました治療薬候補品でした。重症敗血症への適用を考え、第Ⅲ相試験まで到達しました。2011年に開発は中止していますが、「エリトラン」を、COVID–19の感染が確認されて入院中かつ症状が進行している患者さまに適用したいという試みです。
スライドに作用機序とシェーマをお示ししています。「エリトラン」のターゲットはサイトカインを産生するシグナリングの最上流に位置づけるTLR4です。アンタゴニストの役割を果たすということです。
サイトカインは、産生シグナリングの最上流でこの流れを止めるため、下流のサイトカインストームやTNFα、IL-1βなどのサイトカインの産生を一気に抑制する可能性があります。この仮設で、COVID–19の一定の症状の患者さまに「エリトラン」の適用を追求していきたいと考えています。
米国のREMAP–CAP–COVIDという国際的なネットワークで、「エリトラン」のようなドラッグリパーパシングで複数の薬物を評価する枠組みがつくられています。こちらに参画して「エリトラン」の可能性を追求します。
また、来月から国際共同治験(ランダム化比較試験)がスタートします。国内の治験サイトの確保については現在調整中です。現在準備中ですが、約400症例のランダム化比較試験を予定しています。順調にいくと、本年の年末あたりには結果が判明し、第2波、第3波が予想されるCOVID–19に対応する可能性が出てくるのではないかと考えています。
COVID–19 治療薬・ワクチン創出への取り組み(2)
また、当社は顧みられない熱帯病を通じて、ゲイツ財団ともさまざまなコラボレーションを遂げてきました。その関連もあり、ゲイツ財団が中核となっているワクチンの開発にも当社のボストン研究所で創生した免疫アジュバンド「E6020」の可能性を追求しています。
また、治療薬はサンディエゴのスクリプス研究所で、パンデミックReSPONSEライブラリー構築が進んでおり、すでにエーザイの大変ユニークな天然物化合物ライブラリーを提供している状況です。
そして、ロイバント社にすでに導出している「抗GM–CSFモノクローナル抗体」があります。これは、ペンシルベニア州のエクストンにあります旧モルフォテックで創生したアンチボディーです。「抗GM–CSFモノクローナル抗体」は、ロイバント社で急性呼吸窮迫症候群(ARDS)に対する治験が始まっています。私どもは、当社の「エクストン」のファシリティーを用いて、この抗体の原薬製造を行なっています。
ステークホルダーズ支援
ステークホルダーズの支援をこのスライドでお示ししています。国内では、hhcというコンセプトの下に、さまざまな団体やグループと交流しています。例えば、認知症の連携協定を結んでいる自治体や医師会は全国で約167団体に上ります。あるいは、認知症、がん、てんかん、睡眠障害などの患者さまやご家族の100を超える団体ともお付き合いをしています。これらすべて合わせて300団体以上に対して、自分たちの製品やマスク類などを整え、物質の支援を行なっています。
米国、欧州、中国、アジア、アフリカ地域では資金を提供し、感染症保護具を購入していただいたり、第一線の医療機関の支援を行なっています。中国でも早々に武漢市の慈善総会に寄付を行なっています。
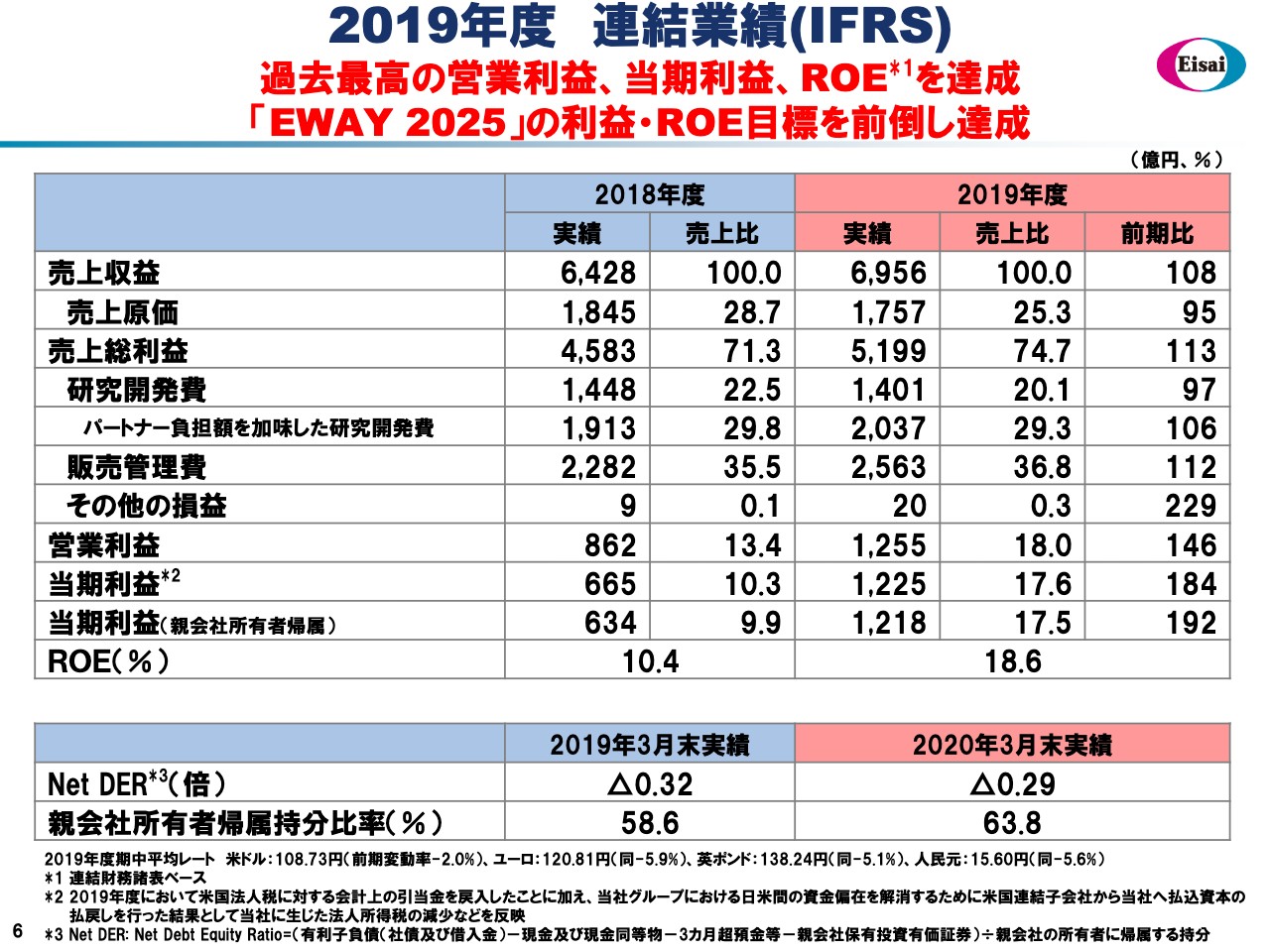
2019年度 連結業績(IFRS)
2019年度の業績について、6ページにお示ししています。この業績の大きな特徴はヘッドラインに記載しました。営業利益1,255億円、当期利益1,225億円、当社持ち分で1,218億円、ROE18.6パーセントと、いずれも過去最高益を記録しました。2010年度において営業利益が1,131億円、ROEが16.4パーセントでしたが、それを超える結果を残しました。売上収益は6,956億円、前年同期比108パーセントとなりました。のちほど詳細にご説明しますが、グローバルの自社品ブランドが大きく成長したことが主な要因です。
売上原価も自社品の成長によるミックスの改善により、3.4ポイント改善しました。売上総利益は堅調に2桁伸びました。研究開発費は前期比97パーセントとなっていますが、常々ご案内していますように、パートナーの分担部分を加えると2,037億円、106パーセントとなり、熱い研究開発資源の投入を行なっています。また、販売管理費は前期比112パーセントとなっています。また、営業利益1,255億円、前期比146パーセント、当期利益1,225億円、前期比184パーセントの実績を確保しました。
スライドの下段に財務の状況を示していますが、Net DERはマイナス0.29で、ネットキャッシュ実質無借金という状況です。そしてこの間、配当総額を上回る600億円を超えるフリーキャッシュを得ている状況です。また、親会社所有帰属持分比率も63.8パーセントであり、いかなる状況下においてもびくともしない財務構造を有しています。
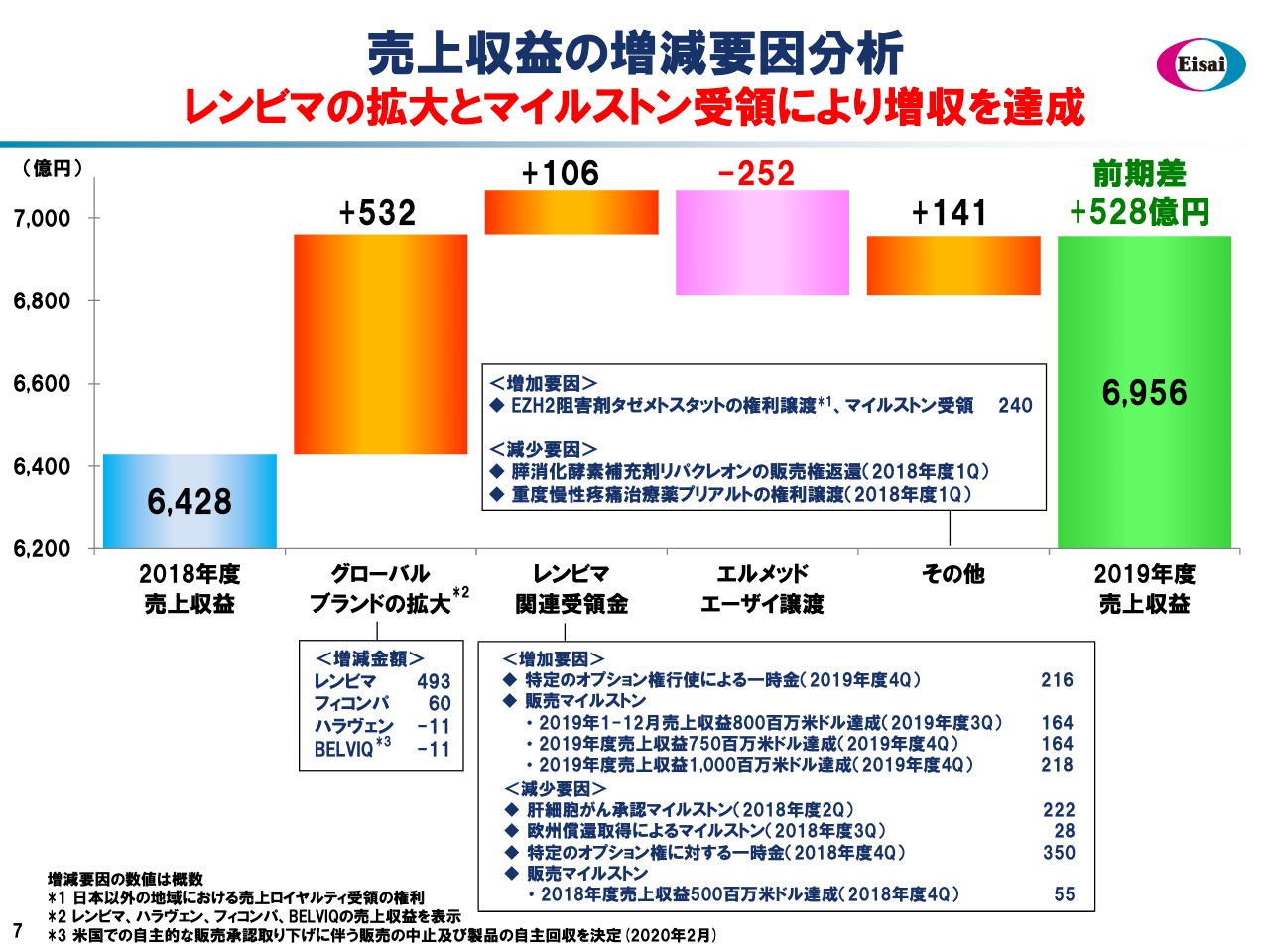
売上収益の増減要因分析
売上収益の状況をご説明します。グラフでおわかりいただけますように、増収の大きな理由は、グローバルブランドの拡大で532億円のアップサイドがあったことと、それにともなう全面のビジネスから得たマイルストンペイメントが、前年に対して106億円増えたことです。
レンビマ関連受領金では、設定しましたすべてのマイルストンをクリアし、前期に対してプラス106億円のマイルストン収入を得ています。また、エルメッドエーザイ譲渡がありましたので、その売上分が減額されました。その他としては、タゼメトスタットの権利譲渡やマイルストン受領などがあり、全年同期比141億円の増額を得ました。これらより、前期差プラス528億円の6,956億円となりました。
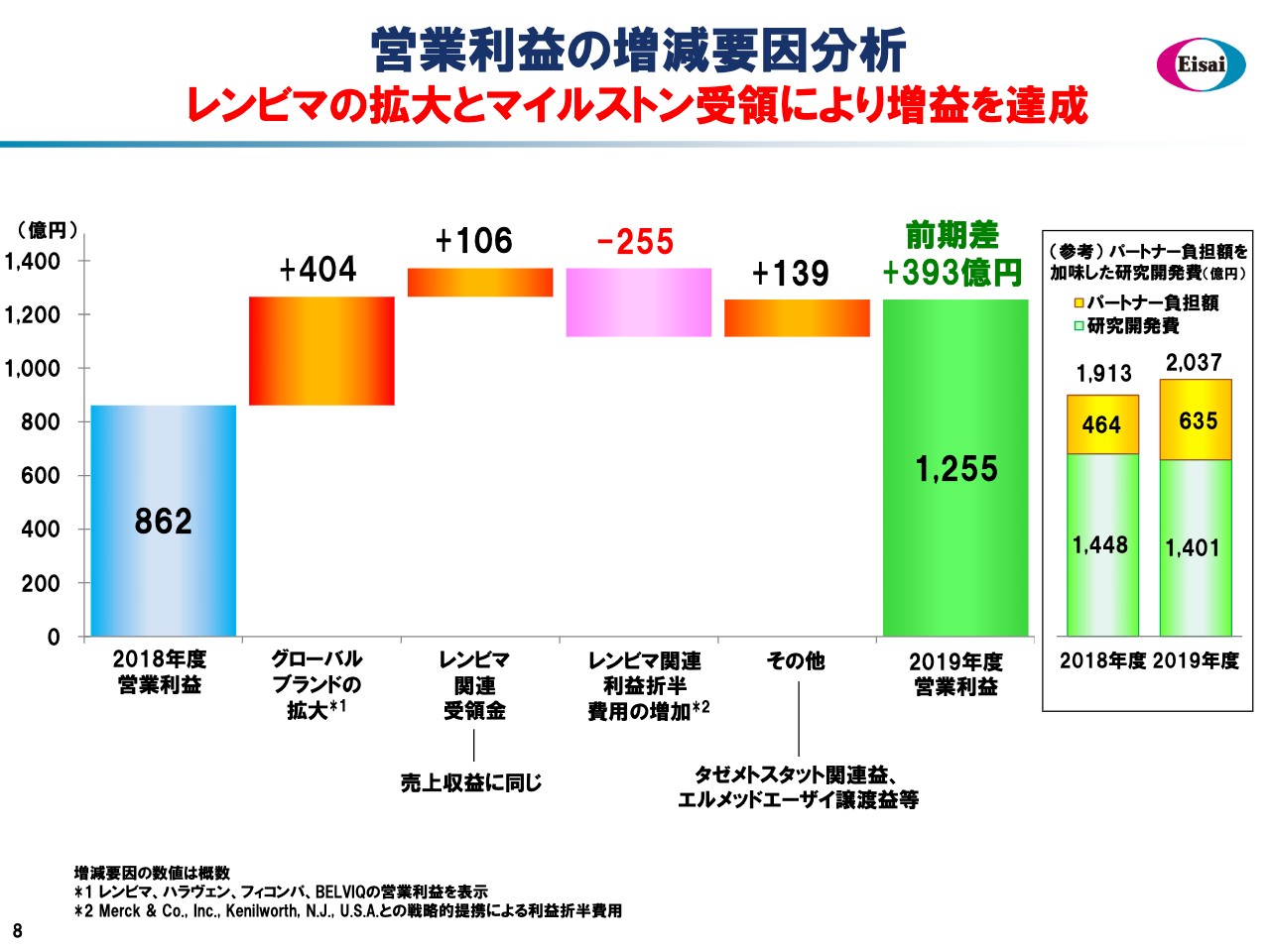
営業利益の増減要因分析
営業利益の要因もほぼ同一です。レンビマ関連利益折半費用の増加という項目でマイナス255億円をお示ししていますが、これは「レンビマ」の拡大によるパートナーへの利益折半の上昇であり、前向きな費用であると考えています。以上の結果、前期差プラス393億円の1,255億円という最高益に到達しました。
スライド右側に研究開発の資源等による様子をお示ししています。2019年度は、P/Lにお示しした1,401億円に、パートナーの分担部分635億円を加えた2,037億円が実質的な研究開発費の投入資源になります。売上比率は約29パーセントで、前年度と比較して106パーセントの上昇です。
レンビマ 2020年度 全リージョンでさらなる患者様貢献拡大
2018年度、2019年度、2020年度と非常に高い成長性を着実に遂げてきました。2020年度は1,580億円、前期比141パーセントというレベルを目指します。その最大のマーケットはアメリカスになります。肝細胞がん、「キイトルーダ」との併用による子宮内膜がんの適応が順調に伸長していることに加え、承認申請中の肝細胞がんのファーストラインの併用療法の上市に向けた準備にも取り組んでいます。
そして二番目に重要なマーケットは中国になりました。新しい患者さま支援プログラムを導入し、患者さまの数が前期に比べて約60パーセント拡大しています。また、甲状腺がんの適用についてもただいま準備中です。本年は日本、欧州、アジア・ラテンアメリカでも子宮内膜がんや肝細胞がんでの上市国の拡大に取り組み、1,580億円に挑んでいきたいと考えています。
レンビマは引き続きがん患者様貢献が拡大
「レンビマ」はさまざまな学会からガイダンスが発出されています。その多くのものは、このCOVID–19の感染リスクの中で内服の抗がん剤を推奨するものです。例えば、一番上のILCAも内服薬を推奨するガイドラインを出しています。また、従来「レンビマ」がCategory2であったものを、Category1として推奨しています。
RCCにおいても、内服の抗がん剤を推奨するガイダンスが出ており、「レンビマ」「エベロリムス」の併用が推奨されることになっています。子宮内膜がんも「キイトルーダ」について、3週間間隔ではなく6週間間隔の投与が推奨され、コンビネーションの療法も伸びている状況です。やはり「レンビマ」が持つ内服抗がん剤としてのメリットが、COVID–19の感染リスクがある中で高まっていると考えています。
コンバージョン療法が世界に浸透 レンビマによる肝細胞がん治療の変革
コンバージョン療法とは、肝細胞がんにおける高腫瘍量の患者さまや、BCLC–Bの中等度の患者さまに「レンビマ」を先行投与して腫瘍量を減少させたのち、TACEなどの根治治療に結び付け、キャンサーフリーを実現していくことです。このコンバージョン療法は、肝細胞がん治療の最高峰である日本であみ出された療法ですが、これがいまグローバルにしっかりと拡大しており、グローバルな学会がそれを支持しています。
レンビマ+キイトルーダ併用療法の進行
「レンビマ」と「キイトルーダ」の併用療法、あるいは第Ⅲ相試験、307試験、309試験などが進行していますが、スライドの左側の5つの試験については、すでに目標症例数の登録が完了しています。307試験、309試験それぞれ多くの症例が集積されている状況です。今後このフォローをしっかりと遂げながら、COVID–19下でも大きな遅れがきたされないように取り組んでいきたいと思います。また、その他の試験についてもフレキシブルに影響を最小化する努力を積み重ねていきたいと思っています。
速やかな入眠、睡眠維持をお届けし、日中の活力ある生活と、リワーク/リカバリー実現を目指す デエビゴ
ニューロジー領域についてお話しします。まず「デエビゴ」です。オレキシンのデュアルインヒビターということで、日米で承認要件をすべて満たし、「ready to go」の状態になっています。オレキシンのバイオジーについては、我が国を代表する研究者である柳沢正史博士により、オーファンGPCR HFGAN72のリガンドオレキシンが発見され、そのオレキシンが睡眠覚醒を制御する重要な物質であることが見いだされました。
この発見に基づいて、筑波研究所でGPCRフォーカスドライブラリーを構築し、「レンボレキサント」を得ました。プラセボ対照試験と高齢者を対象としたゾルピデムERという2つの大規模フェーズⅢ試験で、大変優れた入眠効果と睡眠の質が確認されています。健常成人の2つの試験で、翌日のふらつきおよび記憶力などの持ち越し効果について、プラセボ投与群と比較して問題となるような変化は見られませんでした。米国では添付文書に書き込まれています。入眠効果、睡眠の質、持ち越し効果の3拍子がそろった睡眠障害治療剤が「デエビゴ」であると考えています。
現在、このローンチング準備をしていますが、COVID–19下で従来のように直接医療機関を訪問する情報伝達は大変困難な状況にあります。ここでは、Web上でのMRと医師との面会、あるいはインターネットライブセミナー、デジタル会議を活用したデジタルを中核地とする情報伝達を実行したいと考えています。現在、6月に米国のローンチング、7月の初めに日本における新発売を計画しています。
Aducanumab 申請完了に向けて順調に進捗
「Aducanumab」についてです。申請完了に向けて順調に進捗していることをご報告します。米国においてOpen BLAでモジュールごとの申請を行なっています。この申請プロセスは良好かつ順調に進捗しています。そしてこの夏には、そのOpen BLAのモジュールによる申請の総まとめとも言えるPre–BLAミーティングが正式に設定されています。
私どもは、BLAの申請完了が2020年度の第2四半期に実行できることが明確に視野に入ったと考えています。同時に日本・欧州でも規制当局との協議が継続して進行している状況です。バイオジェン社とエーザイの非常に強固なコラボレーションにより、世界初となるアルツハイマー病の進行抑制剤の貢献実現の本格的な準備を進めています。
BAN2401の進捗
「BAN2401」の進捗です。フェーズⅢ試験Clarity ADについては、順調に症例登録を重ねてきましたが、やはりCOVID–19の影響で、残念ながら現在エントリーのペースが落ちてきています。しかしながら、中国のサイトはまもなく実際の症例登録を開始するところです。エントリーの影響はおそらく3ヶ月ほどではないかと考えており、Final readoutを2020年度の第2四半期に変更します。一方、プレクリニカルADに対する第Ⅲ相試験のAHEAD 3–45については、まもなく試験が開始できます。
そのような中で、ご自宅にうかがって薬物を投与する、あるいは評価をリモートで行なうことは、むしろ規制当局が推奨していることでもありますので、このようなメゾットを積極的に活用しながら影響の最小化を図っていきたいと考えています。
BAN2401 201 コア、OLE 2種類の方法で疾患修飾効果を検証
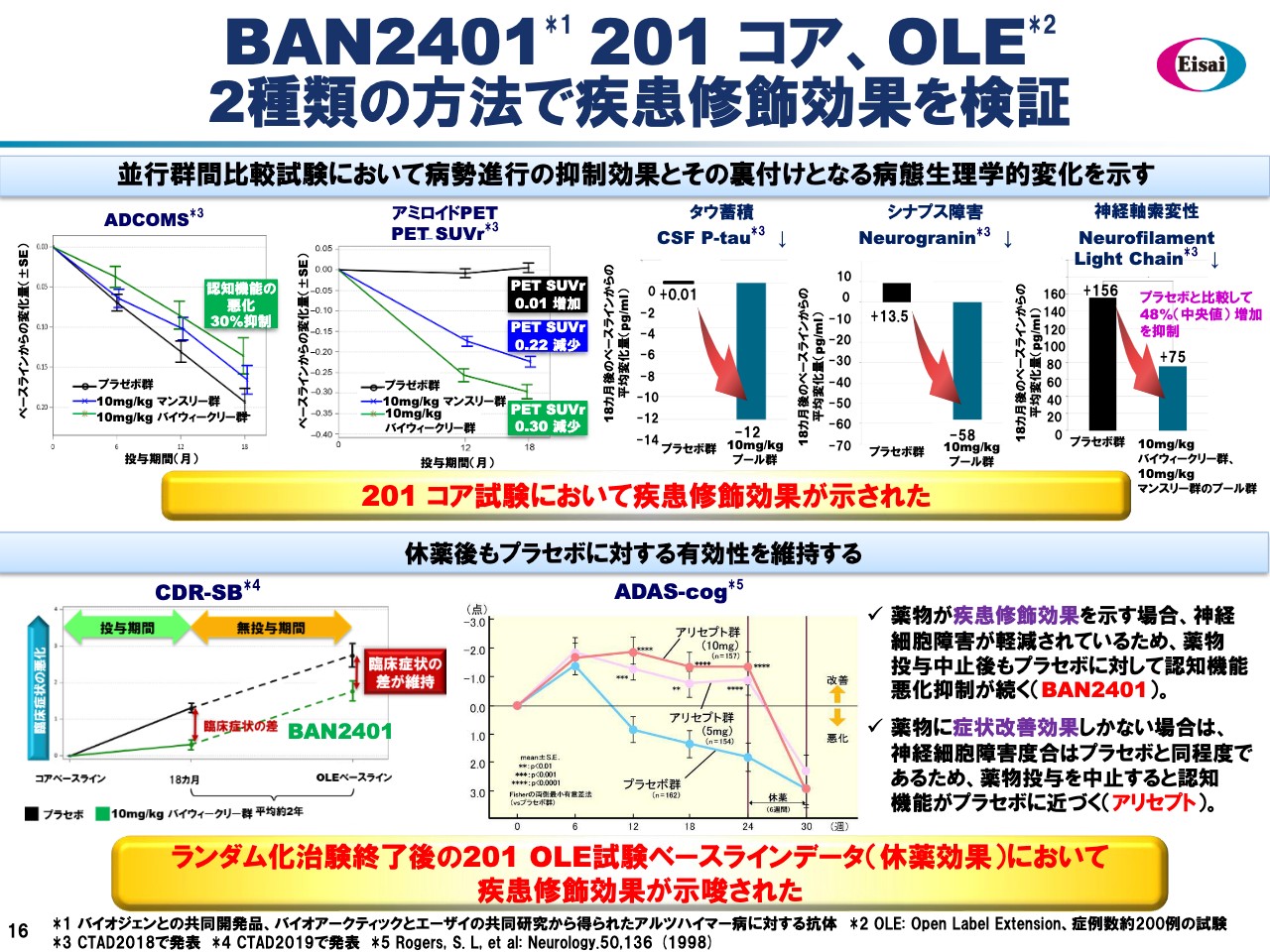
スライドにコア試験、Open Label Extension試験の様子をお示ししています。もちろん201コア試験は並行群間比較試験であり、そこでADCOMSにより進行抑制を証明しました。その背景となる、さまざまなバイオマーカーも同時に病態生理学的に進行抑制を裏付けるものであったことで、201コア試験において疾患修飾効果が示されたと言えると考えています。
一方、OLE試験はランダム化治験終了後約2年間投薬されていません。ここがOLE試験ベースラインのスタートになります。その時点でのCDR–SBによる認知機能の状況をご覧いただきたいと思いますが、コアでの実薬群とでプラス部分の間にありました認知症の悪化抑制効果は維持されています。ともに悪化はしていますが、その差は依然としてしっかり広がっていることが示唆されるデータです。薬物が疾患修飾効果を示す場合、神経細胞障害が軽減されているため、薬物投与中止後もプラセボに対して認知機能悪化抑制が続くことを示唆しており、疾患修飾効果を示す有力なデータになり得るのではないかと考えています。
また、我々の気管薬である「アリセプト」ではどうだったかをお示ししています。アリセプトのコア試験が終わり、6週間の休薬期間を経たあと、実薬群の認知機能の悪化はプラセボ群と同一レベルまで悪化しています。やはり、症状改善効果と疾患修飾効果の違いが明確にあることが示唆されているのではないかと考え、ご紹介しました。
日常生活領域と医療領域の架け橋となる認知症プラットフォームeasiit
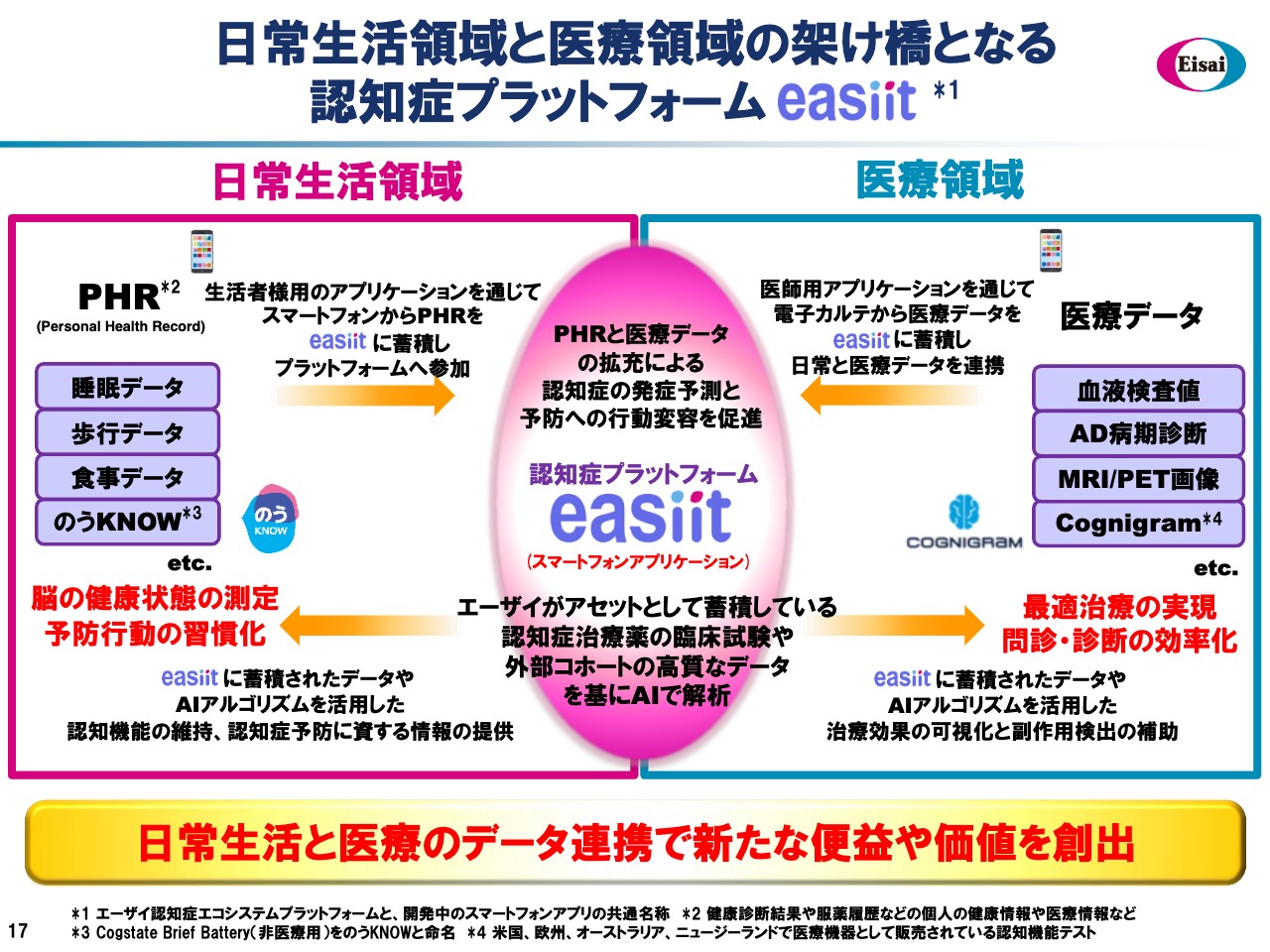
我々はアルツハイマー病治療薬の患者さまへの貢献に本格的に取り組むタイミングにきていることを先ほどお伝えしました。その1つの大変重要な取り組みがこの認知症プラットフォーム「easiit」です。エーザイが「アリセプト」以来蓄積してきた認知症治療薬の中のさまざまなAD DMTのデータや、その臨床試験、外部コホートの高質なデータを基にAIで解析し、さまざまなものを予測したりアドバイスしたりすると、「easiit」のコアアセットになります。
このアセットを活用するために、日常生活領域では生活者のみなさまから、睡眠や歩行の様子、お食事の様子などのいわゆるパーソナルヘルスレコードや、「easiit」の一部として4月より事業社向けに販売開始しました「のうKNOW」というデジタルツールによるブレインパフォーマンスの簡便なチェックなどの情報を、「easiit」に寄せていただき、データをAIで解析し、認知機能の維持や認知症予防に資する情報をお返ししていきます。このループを回すことにより、脳の健康状態の測定や予防行動の習慣化を促進していく狙いです。
一方医療領域は、さまざまな医療機関における血液の検査値などの医療データ、あるいは「のうKNOW」の医療版「Cognigram」という同じアルゴリズムを使ったブレインパフォーマンスの測定法がありますが、このような情報を「easiit」に医師用アプリケーションを通じて電子カルテからインプットしていただき、AIアルゴリズムを活用した治療効果の可視化、あるいは副作用検出の補助などを情報としてお返しします。
これにより、最適治療の実現や問診診断の効率化を図っていくのがこの認知症プラットフォーム「easiit」の全体像になります。つまり、日常生活と医療のデータ連携で新たな便益や価値を創出するようなプラットフォームが「easiit」であると言えます。
easiitによるキャズムの解消
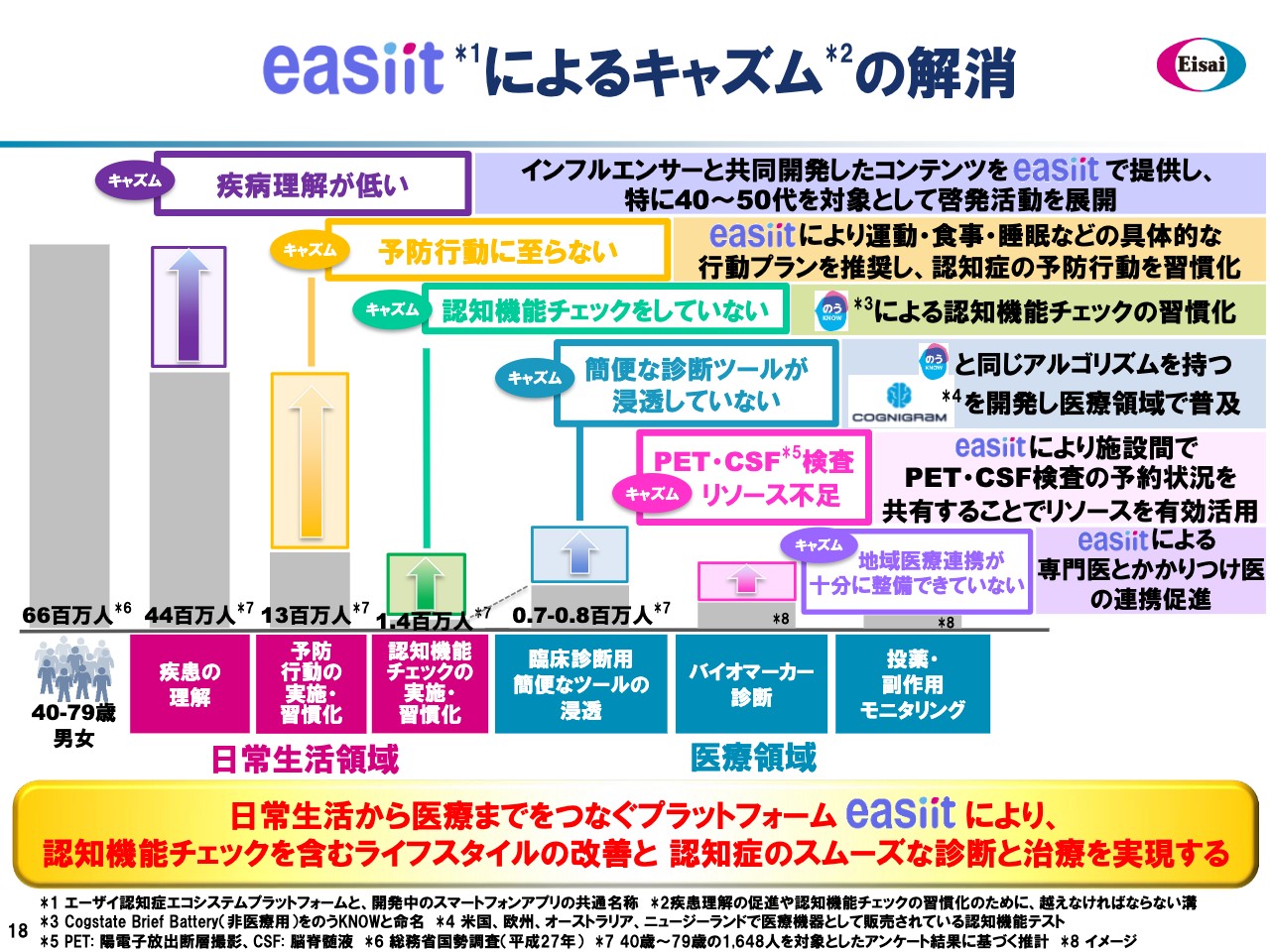
キャズムとは、疾患理解の促進や認知機能チェックの習慣化のために、越えなければならない溝のことです。全体のポピュレーション約6,600万人のうち、疾患の理解をしている方は4,400万人です。予防行動を実施したり、習慣化している人はもっと減りますし、認知機能のチェック、実施・習慣化をされる方ももっと減ってきます。端的に言えばこの差がキャズムです。臨床診断用の簡便なツールの浸透、バイオマーカー診断など、医療領域にいきますとさらに人数は減ります。そして投薬・副作用モニタリングにはもっと大きなキャズムが存在しています。
このそれぞれのキャズムに先ほどお伝えしました「easiit」を用いて、キャズムの解消を図っていきたいということです。例えば、疾患理解が低い方については、40歳代から50歳代の方々にインフルエンスがあるインフルエンサーと一緒に開発したコンテンツを「easiit」で提供して、疾患の啓発活動を行なっていきます。
認知機能チェックをしていない、あるいは簡便な診断ツールが浸透していないところでは、「のうKNOW」や「Cognigram」によって、これを解消していきたいと思います。PET・CSF検査のリソース不足については、施設間でのPET・CSF検査の予約状況などを「easiit」で把握して、それをお使いいただきたいと思います。
「easiit」を使い、地域における専門医やかかりつけ医とみなさまのネットワーク連携の促進を遂げていきます。この「easiit」を用いることにより、認知機能チェックを含むライフスタイルの改善や、認知症のスムーズな診断と治療を実現するためのキャズム解消を図っていきます。
COVID–19のもたらす新秩序 二つの原則:生命が最優先、自国だけでは成り立たない
ニューノーマルと言われているCOVID–19のもたらす新秩序についてです。私どもはこのCOVID–19に直面して、2つの原則があることをあらためて認識しています。1つは生命が最優先であること、もう1つは自国だけよくても成り立たないことです。自分が「OK」でも、相手が「NOT OK」では成り立たちません。
また、COVID–19下の大きな新秩序のキーワードは、やはりデジタルトランスフォーメーションとなっていくと思います。しかしながら、デジタルとパーソナルのコンビネーションをしっかりと考えていかなければいけないと思います。「easiit」もそうですし、新コミュニケーション、デジタルプラットフォームで非常に多くの患者さまと直接双方向のコミュニケーションができます。我々の営業第一線活動もデジタルを使ってフィジカルとのコンビネーションが追求できます。
医療供給体制でもすでに起こっていますように、オンライン診療やヘルスプロフェッショナルの人々の間の遠隔医療、あるいはアフリカなどの遠隔地でも罹患状況等をアプリで把握する、予防活動を展開できる、ということがどんどん進行しています。
スライドの右上に新ロジスティックスと記載しました。先ほどの安定供給のお話です。これからも気候変動は続き、どのようなパンデミックが起こってくるかわかりません。自然災害も起こります。そのような中でマーケットも大きくなったり、小さくなったりしていくことをAIで予測し、原材料の調達から生産計画までをしっかりと実行していきます。そのようなグローバルERPを実現していかなければなりませんし、例えば、原薬中間体から最終製品までグローバルネットワークで作り上げるのではなく、よりリージョンベースでのネットワークの必要性も高まってくると思います。
またスライド右下に新生命関連政策・事業と記載しました。パンデミックだけではなく、AMR、あるいは省みられない熱帯病などが、いつ全世界の大きな疾病として重要性を増すかは予断を許さないと考えています。そのような中で、我々は低所得層や低所得国における問題解決能力を向上することに取り組んでいかなければなりません。例えば、UHC下における給付レベルをどのように上げていくかなどに真剣に取り組んでいかなければと思います。今も議論されていますが、薬事承認制度における優先的審査の柔軟かつ広い適用も重要な項目になっていくのではないかと考えています。
2020年度 連結業績見通し(IFRS)
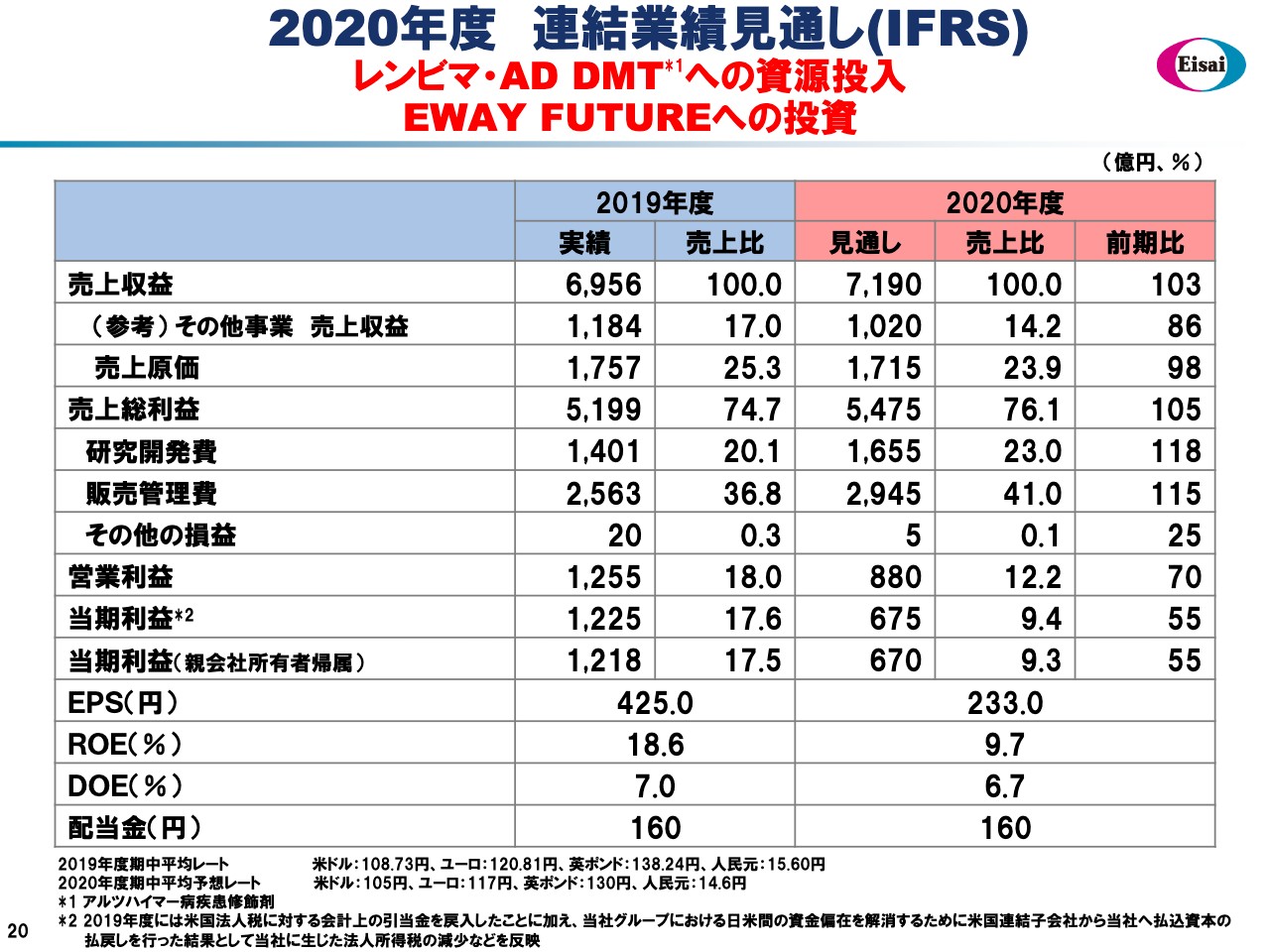
2020年度のP/Lになります。売上高7,190億円、前期比103パーセントで、グローバル品を中心に続伸していく見通しです。その他事業、売上収益にいわゆるマイルストンペイメント1,020億円を予定しています。先ほどお伝えしたように、「レンビマ」は、製品売上の1,540億円とマイルストン収入を加えると約2,200億円となる大きな売上収益を上げる事業に成長してきました。
売上原価は自社品のミックスにより引き続き低減を遂げていきます。売上総利益は前期比105パーセントと堅調なる増益を果たすことになります。研究開発費、販売管理費の費用投入について、2020年度はEWAY FUTUREに向けての投資とご理解していただきたいと思っています。研究開発費においては、「Aducanumab」「BAN2401」をはじめとするAD関連品のいずれも大きなスタディーが進行します。また販売管理費は、「レンビマ」のパートナーへの利益折半分も増額になりますし、AD DMTの患者さま貢献の準備を本格的に実行していく年に入りましたので、そこにも大きな費用投入を行なう予定としています。
そのような先行投資のタイミングということで、営業利益は880億円、当期利益670億円を見込んでいます。ROEは9.7パーセントで、エクイティ・スプレッドをしっかりと確保する年度にしたいと思っています。配当金については、本日の取締役会で2019年度の期末配当80円を決議しています。また、2020年度の配当金も160円を予想しています。以上、2019年度のご報告をさせていただきました。ご清聴ありがとうございました。