2022年2月14日に行われた、サスメド株式会社2022年6月期決算説明会の内容を書き起こしでお伝えします。
スピーカー:サスメド株式会社 代表取締役社長 上野太郎 氏
ビジョン
上野太郎氏(以下、上野):サスメド株式会社代表取締役の上野です。みなさま、本日はお忙しい中お集まりいただき、ありがとうございます。昨年末の上場以来、初めてとなる決算説明会を開始させていただきます。
初めに、私どものビジョンと事業内容をご説明します。私どもサスメド株式会社は、「ICTの活用で『持続可能な医療』を目指す」ということをビジョンに掲げています。その「SUStainable MEDicine」を略して、会社名をサスメドと称しています。
具体的な事業内容についてですが、治療用のアプリ開発で、スライド下部に記載のように「Digital Therapeutics」、もしくはそれを略して「DTx」と言われています。
このDTxのプロダクトを、それぞれの疾患向けに医療機器として開発するのが「DTxプロダクト事業」です。こちらについては、患者さんや医療従事者の方々にお使いいただく仕組みになっています。同時に、私どもはDTxを開発するためのプラットフォームを有しており、こちらを製薬メーカーの方々向けにBtoBで展開する「DTxプラットフォーム事業」も行っています。
事業領域概要
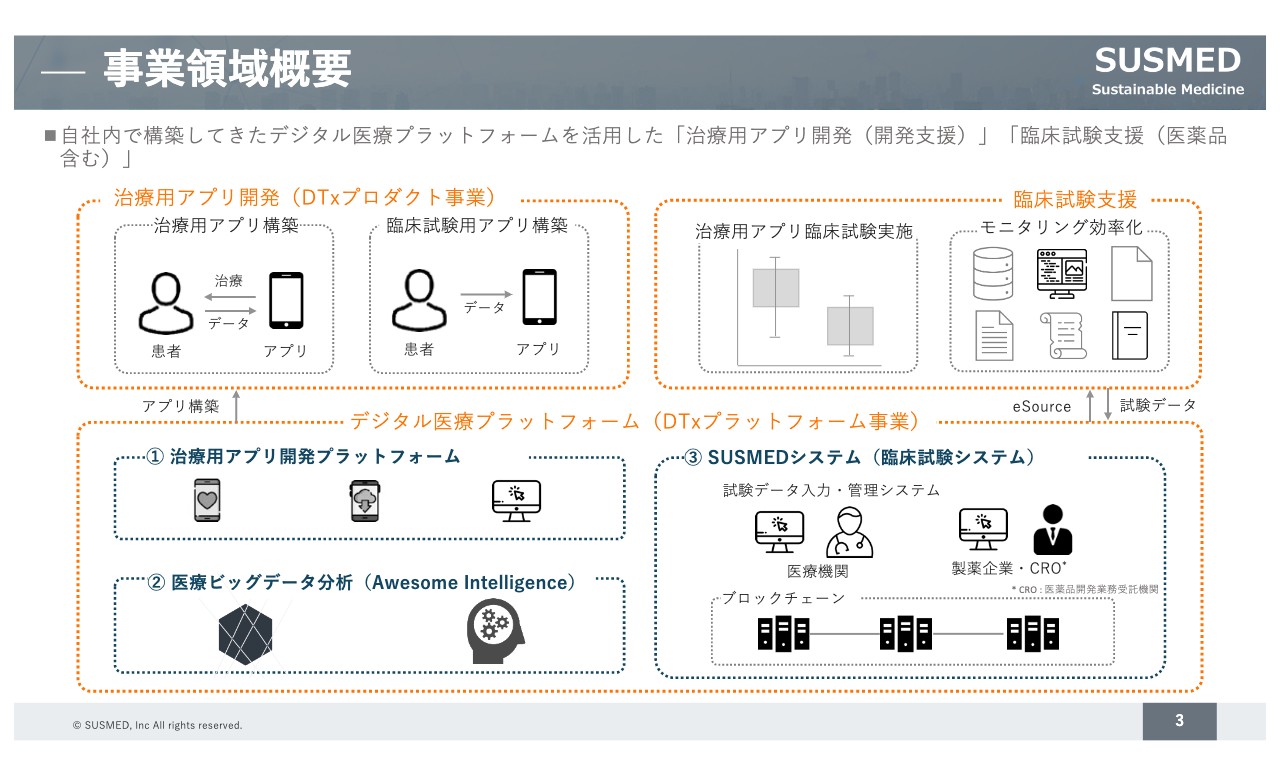
当社の事業領域の概要です。私どもの強みは、スライド下部に記載の「デジタル医療プラットフォーム(DTxプラットフォーム事業)」です。このプラットフォームの中に、弊社が多数保有する特許などが盛り込まれています。
具体的には、スライドの①に記載のように、治療用のアプリを開発するためのプラットフォームの役割があります。また、このような治療用アプリ経由で全国から集まってくる医療ビッグデータを、機械学習を用いてクラウドサーバー上で分析するための仕組みとして、②の医療ビッグデータ分析(Awesome Intelligence)があります。
さらに、臨床試験を効率よく実施するための仕組みとして、当社ではブロックチェーン技術を用いた③のSUSMEDシステム(臨床試験システム)を持っています。後ほど、研究開発費の圧縮の部分と絡めて、少しご説明します。
このようなプラットフォームを活用して、大きく2つの事業を行っています。1つは治療用アプリの開発(DTxプロダクト事業)です。もう1つが、臨床試験の効率化を図るための事業をBtoBで行う取り組みになります。
治療⽤アプリの提供の流れ
治療用アプリに関する「DTxプロダクト事業」からご説明します。この治療用アプリは医療機器に該当するもので、医薬品や医療機器と同じように、疾患を治療するために用います。
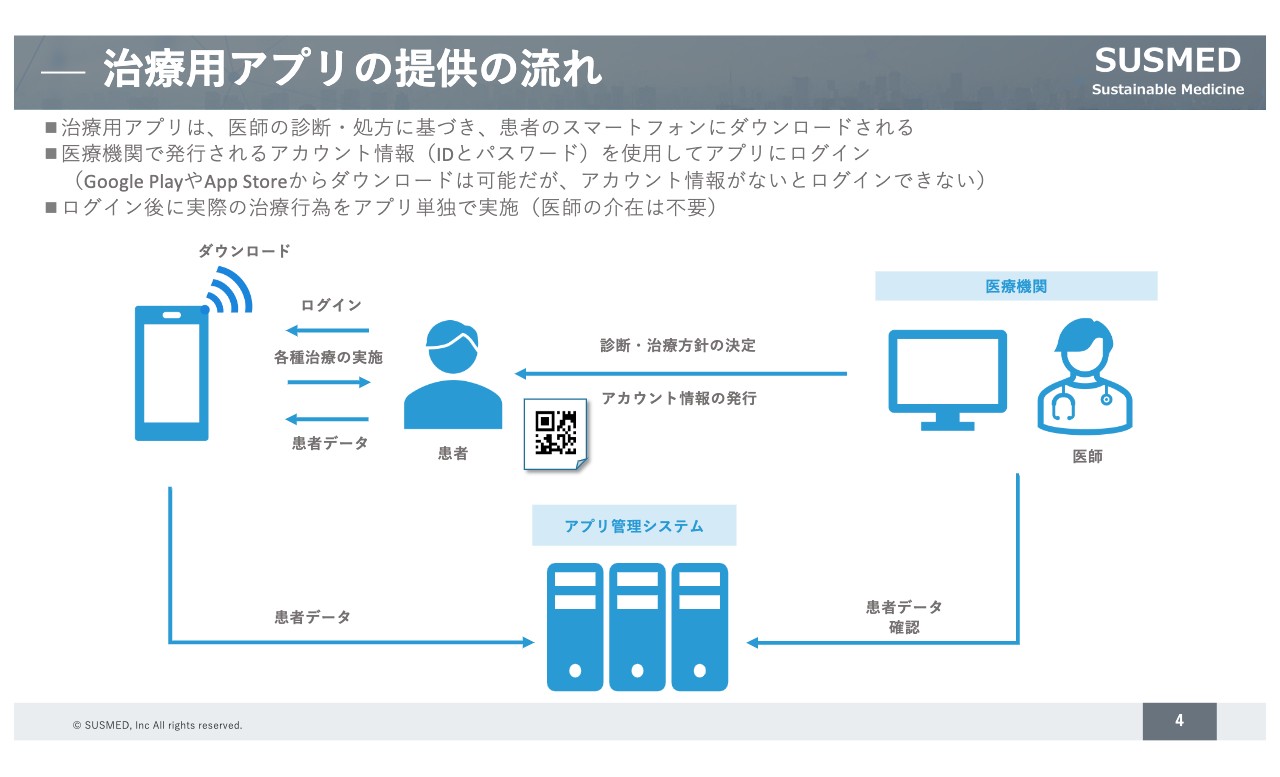
医療行為については、基本的に医師の監督のもとで行うため、治療用アプリはコンシューマ向けのアプリと違い、医師が患者に対して処方し、患者はご自身のスマートフォンでログインして治療を受けるという医療機器になっています。そのため、医療機関で発行されるアカウント情報がなければログインできない仕組みになっています。
また、遠隔診療などとは異なり、ログイン後の実際の治療行為については、裏側に医師は必要なく、基本的にはアプリ単独で治療行為を行う仕組みになっています。
また、治療用アプリ経由で集まってくる患者のデータを医療機関の医師が確認することで、診療行為を効率化する仕組みにもなっています。
ヘルスケアアプリと治療⽤アプリの違い
世の中にヘルスケアアプリは多数存在していると思いますが、私どもの治療用アプリは、疾患を治療するものです。用途として治療を謳うものであり、薬機法の規制の対象になります。そのため、医学的エビデンスに基づいた厚生労働省の承認が必要になります。
医療機器として認められ保険収載されることで、医療保険によって患者さんの負担する費用が、例えば3割ほどに軽減されるなど、そのようなかたちで患者さんの治療に用いることができる仕組みになります。
一般的なヘルスケアアプリの場合、医学的なエビデンス等はなく、基本的には血圧などを記録するものになっていますが、治療用アプリは疾患を治療することが可能な医療機器です。私どもも治験を実施し、医学的なエビデンスを取得した上で厚生労働省に承認申請し、承認を得ることが必要になります。
治療用アプリは医師の処方のもとで患者さんの治療に用い、また医師へのマーケティングを行うことで、全国に展開する仕組みになっています。医療機器として保険適用の事例もすでに先行して出てきており、保険を使って患者さんの治療を進めることができるようになっています。
開発パイプライン
当社の開発パイプラインです。不眠障害の治療用アプリについては、2022年2月1日に厚生労働省に対する承認申請が完了しています。PMDAに事前に相談し、その上で問題ないということで、承認申請しているものです。また、直近にアップデートがあったものについて赤文字でお示ししています。
ACPについては、探索的試験が現在進行中になります。ACPというのは「Advance Care Planning」の略です。中身としては、進行がんの患者に対して、治療方針の意思決定支援を行う取り組みです。後ほど、こちらについても少し触れます。
その他、アップデートがあった点は妊産婦うつの診断機器への取り組みです。こちらについては、アルゴリズムおよび装置に関する特許が成立しています。
外部環境の変化
外部環境の変化について少し共有したいと思います。先日、令和4年度の診療報酬改定が厚生労働省から発出されています。その中で、私どもの事業と関連するものをピックアップしてご案内します。
1点目は、プログラム医療機器に関する管理料が新設されました。これによって、プログラム医療機器、治療用のアプリを処方して管理することについて、医療機関側に対するインセンティブとしての診療報酬がきちんと付くようになっています。そのため、プログラム医療機器の普及が後押しされる状況になっています。
2点目は、先ほどお伝えしたACPと関連して、がん患者指導管理料の見直しがされています。もともと、がん患者指導管理料というものがあったのですが、その中に新設されるかたちで、「末期の悪性腫瘍の患者に対して、当該患者の診療⽅針等に関する意思決定⽀援を実施した場合にも算定可能とする」と追記されました。
この見直しから、「Advance Care Planning」についても保険償還の対象になるという流れができています。こちらは、欧米や台湾などではすでに保険点数が付いている取り組みになっています。それが日本でも追いついてきたという状況です。
3点目は、ハイリスク妊産婦連携指導料の見直しが実施されています。妊産婦の方々の連携指導料は、もともと診療報酬にありましたが、これまでは「精神療法を受けている妊産婦に限る」とされていました。
それが今回、現時点で精神療法を受けている妊産婦に限らず、「メンタルスクリーニング検査等により精神科⼜は⼼療内科の受診が必要と判断された患者を追加する」というかたちになっています。まさに、妊産婦うつの患者の診断に対するニーズが顕在化しており、私どもの取り組みが連携指導料の面でもサポートいただける状況になってきています。
4点目に、透析中の運動指導に関する評価も新設されています。私どもは、慢性腎臓病患者に対してのアプリ開発にも取り組んでいますが、人工腎臓を算定している患者に対しても腎臓リハビリの評価が新設されており、腎臓リハビリの保険償還対象となる患者が拡大する流れがあります。
このように、診療報酬改定について、来年度の令和4年度に4点の新設や追加が実施されるため、外部環境の追い風が吹いてきている状況です。
汎⽤臨床試験システム:SUSMEDシステム
ここまでは治療用アプリ開発(DTxプロダクト事業)についてお話ししてきました。続いて、プラットフォーム事業による臨床試験の効率化についてご説明します。
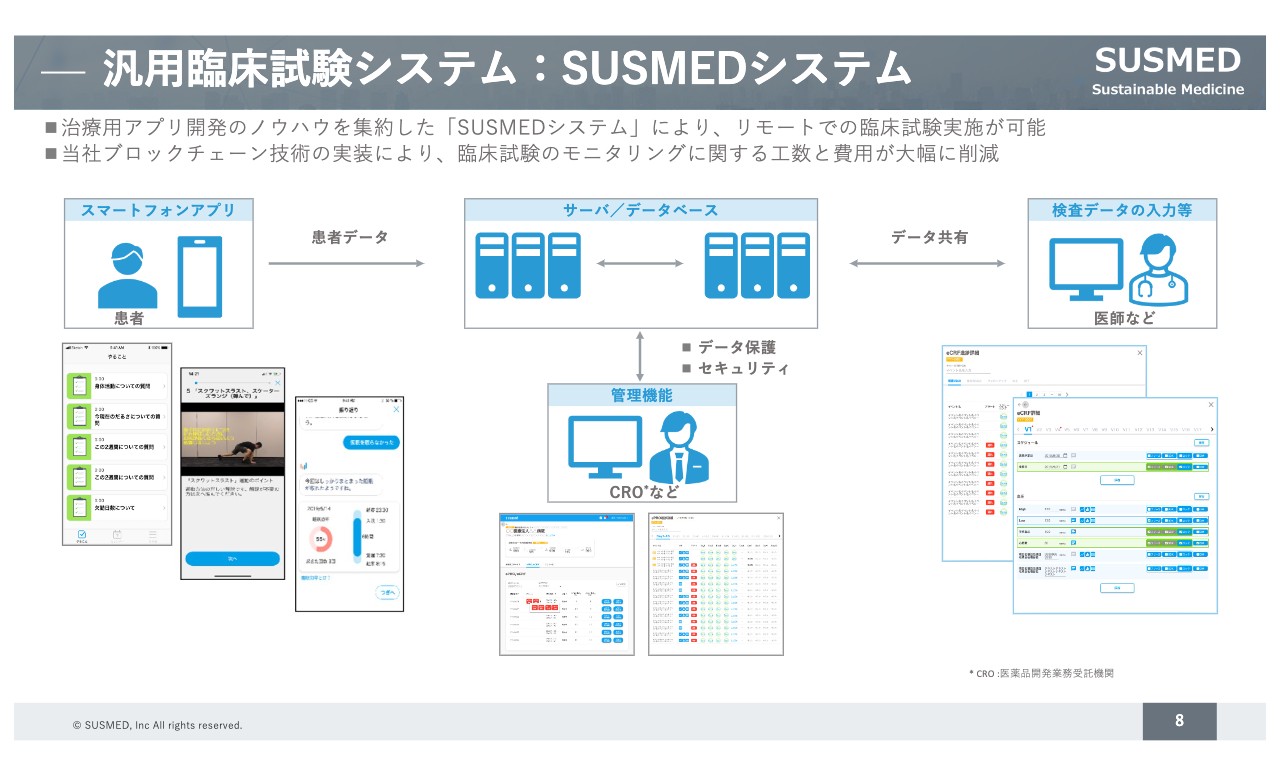
当社では治療用アプリの開発のノウハウを有しています。それを実際に、汎用の臨床試験システム「SUSMEDシステム」として、BtoBの事業に展開しています。この仕組みを使うことで、リモートでの臨床試験が実施可能になる仕組みです。
さらに、当社が保有している特許技術である、ブロックチェーン技術を臨床試験で用いることにより、臨床試験のモニタリングに関する⼯数と費⽤が⼤幅に削減可能となります。
臨床試験の場合には、データの信頼性を担保しなければいけないというレギュレーション対応が必要ですが、そのモニタリングを、これまで人が行っていた部分を、ブロックチェーン技術で担保する技術を実装することで、臨床試験のコストを大幅に削減できる仕組みになっています。
ブロックチェーン技術の実装による効率化
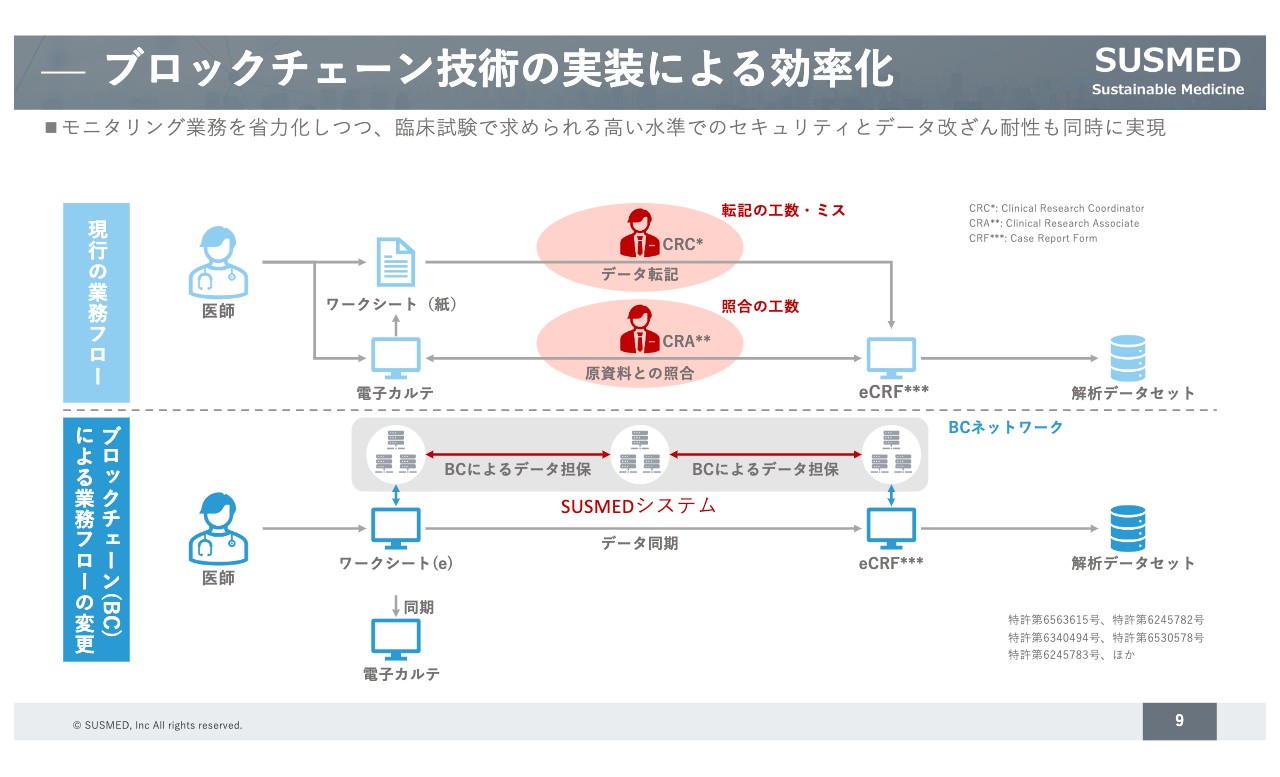
こちらは、ブロックチェーン技術を実装することによる臨床試験の効率化を図示したものです。
現行の業務フローをスライド上部にお示ししています。医師が電子カルテに入力した診療情報を、治験の場合にはデータ転記し、eCRFと呼ばれる症例報告書を作ります。
この「症例報告書のデータの真正性を担保しなさい」というGCP省令というレギュレーションがあり、こちらに対応するため、従来はCRO(医薬品開発業務受託機関)から派遣されたCRA(Clinical Research Associate)という方が、原資料との照合作業を業務として行っています。SDV(Source Date Verification)とも言われる業務ですが、実際に医療機関を訪問して、電子カルテのデータと症例報告書のデータを1つずつ照合作業するのが、これまでの業務フローになっています。
非常に労働集約的なかたちになっており、CROの方々の単価が1人月あたり200万円ほどかかるため、非常に治験のコストがかかる理由になっています。それに対して、私どもの特許技術であるブロックチェーン技術を用いた仕組みは、医療機関側のデータをブロックチェーン経由でeCRFにつなぎ込みます。
みなさまご存じのように、ブロックチェーンの技術は、もともと仮想通貨などで使われ始めた技術で、データの改ざんを非常に困難にするという特徴があります。最近ではWeb3.0などでも話題になることがありますが、データ改ざんが不能であるというブロックチェーンの特性を活かすことにより、医療機関側のデータと当局に提出する症例報告書のデータの信頼性を担保し、CROの業務を削減する仕組みを構築しています。
機械学習⾃動分析システム:Awesome Intelligence
その他にも当社では、これから治療用アプリで集まってくる医療ビッグデータや、あるいは製薬企業の方々がすでに保有している医療ビッグデータを、私どものクラウドサービスで分析する仕組みも保有しています。
このサービスを使うことで、製薬企業向けのtoBのサービス提供や、これから集まってくる医療ビッグデータの分析を、人手をかけずに実施していく予定です。ここまでが当社の事業のご紹介となります。
2022年6⽉期 重点施策
2022年6月期の重点政策について進捗をご説明します。大きく3点あり、1点目が不眠障害治療用アプリの製造販売承認申請、2点目がブロックチェーンによる臨床試験システム稼働実績の蓄積、3点目が上場によって研究開発資金を調達する取り組みになります。
重点施策①不眠障害治療⽤アプリの製造販売承認申請
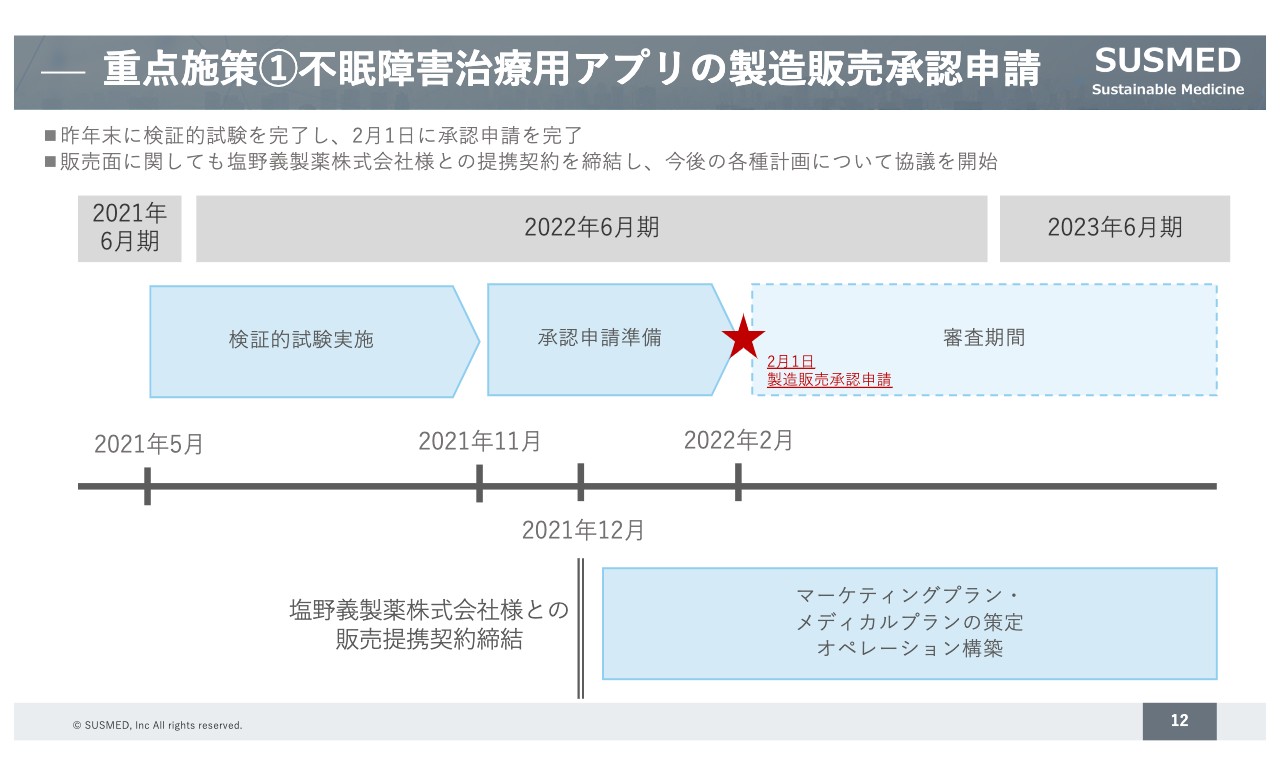
まず1点目の不眠障害治療用アプリの製造販売承認申請についてです。先ほどお伝えしたように、2月1日付で医療機器の製造販売承認申請を完了しています。PMDAには、事前に相談した上で承認申請を行い、特段問題がないとのことで申請完了に至っています。
加えて、販売については、特に精神科領域に強みを有している塩野義製薬さまと販売提携契約を締結しています。こちらの契約締結後に、マーケティングプランやメディカルプラン、オペレーション構築などの部分で協業を進めています。
重点施策②臨床試験システム稼働実績の蓄積
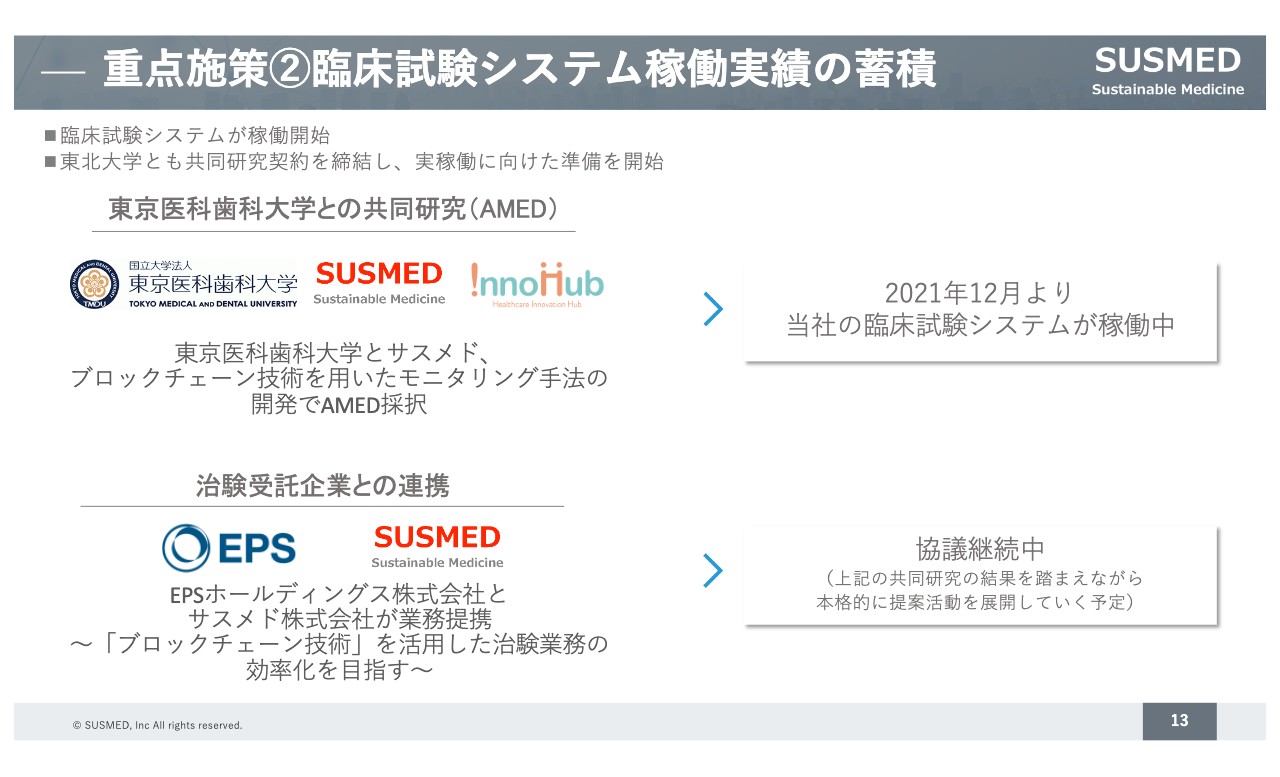
2点目の、ブロックチェーンを含む臨床試験システム稼働実績の蓄積についてです。AMEDのプロジェクトとして実施している、東京医科歯科大学さまとの共同研究においてブロックチェーンシステムが稼働しています。2021年12月から当社の臨床試験システムが稼働し、臨床試験を実施しているかたちです。
また、CROの最大手であるEPSさまと、ブロックチェーン技術を用いた効率的な治験を目指して業務提携しており、こちらについては協議を継続しています。さらに、先日リリースしていますが、東北大学さまとも、私どものブロックチェーンの技術を用いた共同研究契約を締結し、実稼働に向けた準備を進めています。
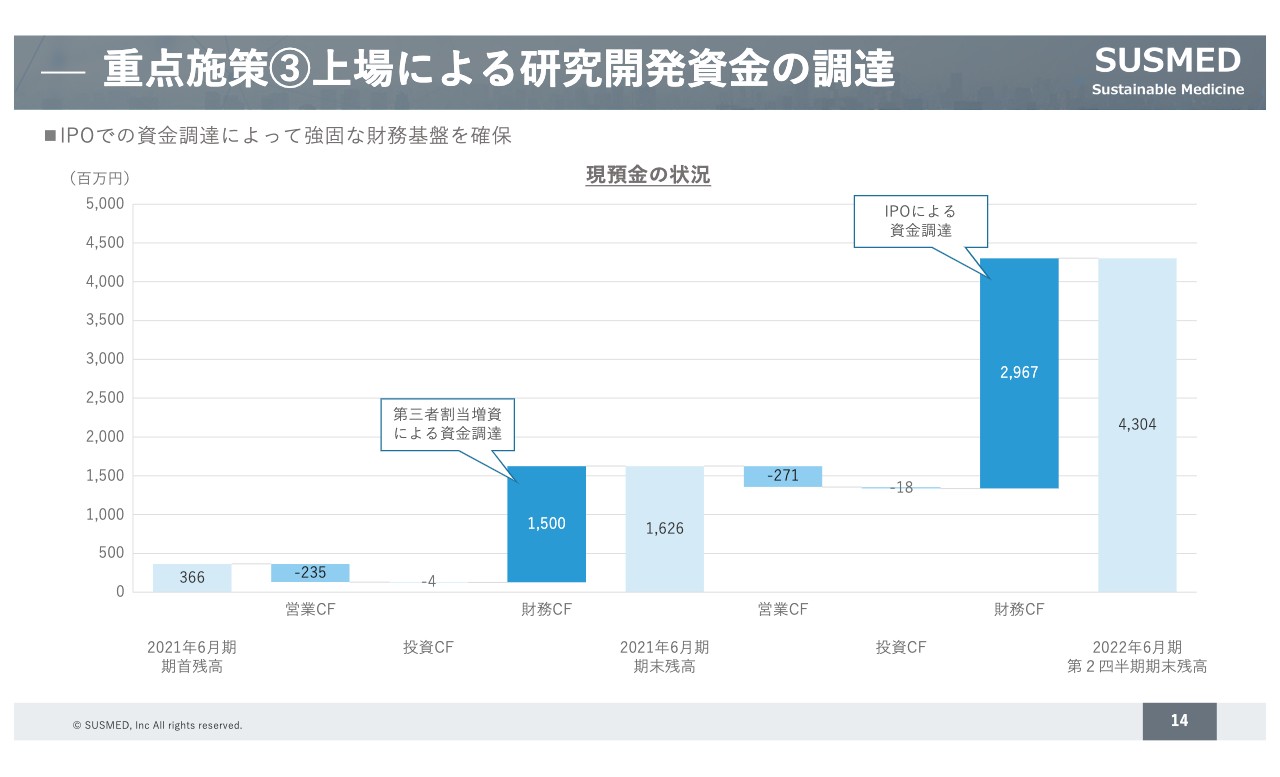
重点施策③上場による研究開発資⾦の調達
3点目の研究開発資金の調達では、上場の部分についてご説明します。ご承知のとおり、私どもは昨年末のIPOの際に資金調達させていただいています。これにより、強固な財務基盤を確保している状況です。
2022年6⽉期 重点施策の現在地
繰り返しのご説明になりますが、今期の重点施策において、不眠障害の治療アプリについてはスケジュールどおり承認申請し、塩野義製薬さまとの販売提携を実施しています。臨床試験のシステムでは、東京医科歯科大学さまとの取り組みが稼働しはじめ、他大学や他企業との取り組みも今まさに動いているところです。
また、上場による研究開発資金の調達は、積極的な研究開発活動の推進を可能にするための財務安定性を獲得しているというのが、現在のステータスになります。
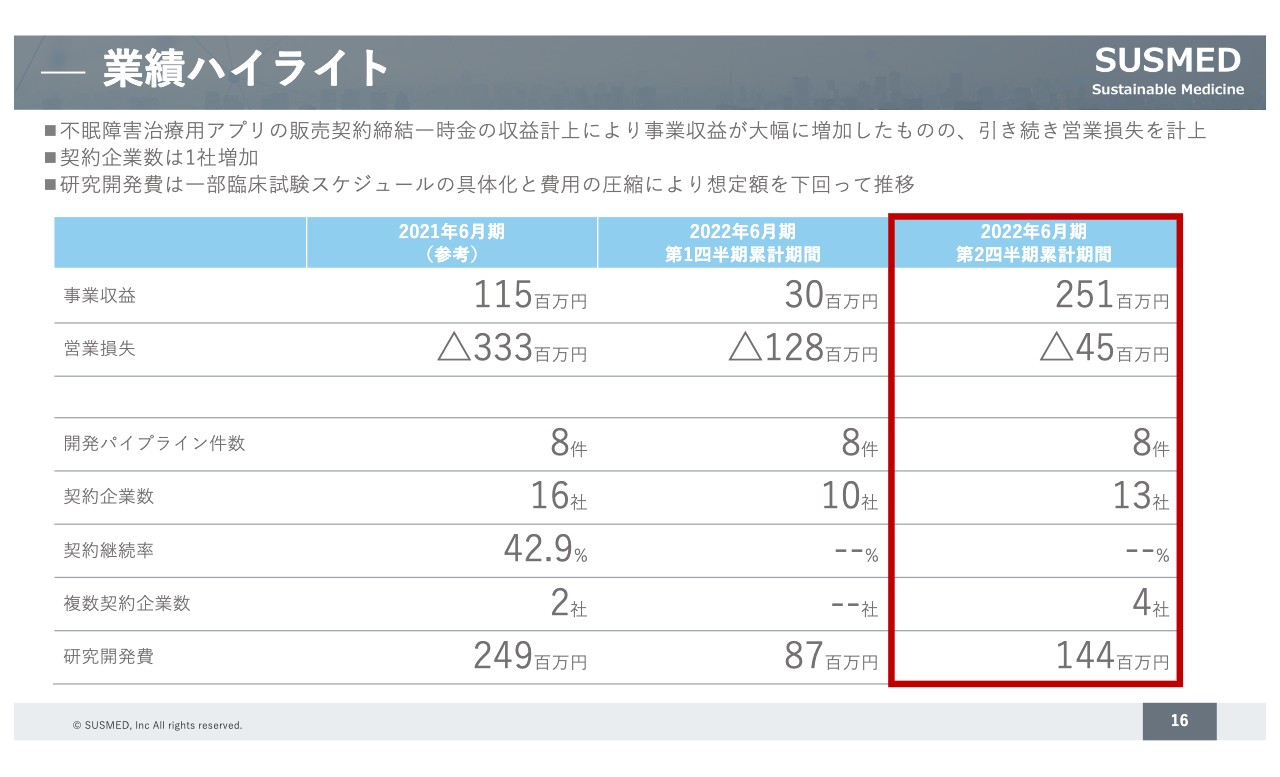
業績ハイライト
業績ハイライトです。まず、2022年6月期第2四半期の部分ですが、事業収益は2億5,000万円で、塩野義製薬との販売提携の締結一時金の収益により、2億円を計上しています。営業損失はマイナス4,500万円となっています。研究開発費は当初予定よりもかなり圧縮できています。
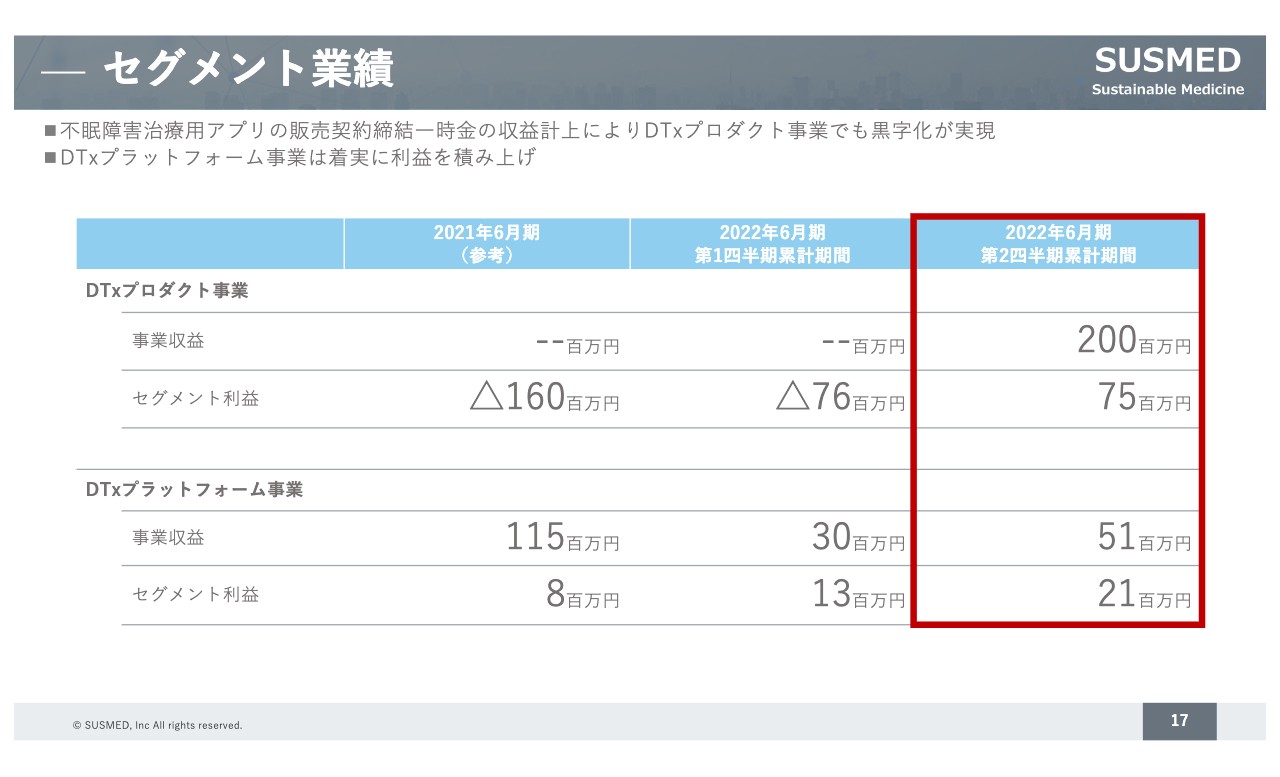
セグメント業績
セグメントごとの業績です。DTxプロダクト事業の収益については、先ほどお伝えしたように、塩野義製薬からの契約一時金の受領で2億円となっており、セグメント利益は7,500万円です。DTxプラットフォーム事業は5,100万円の収益、セグメント利益が2,100万円となっています。
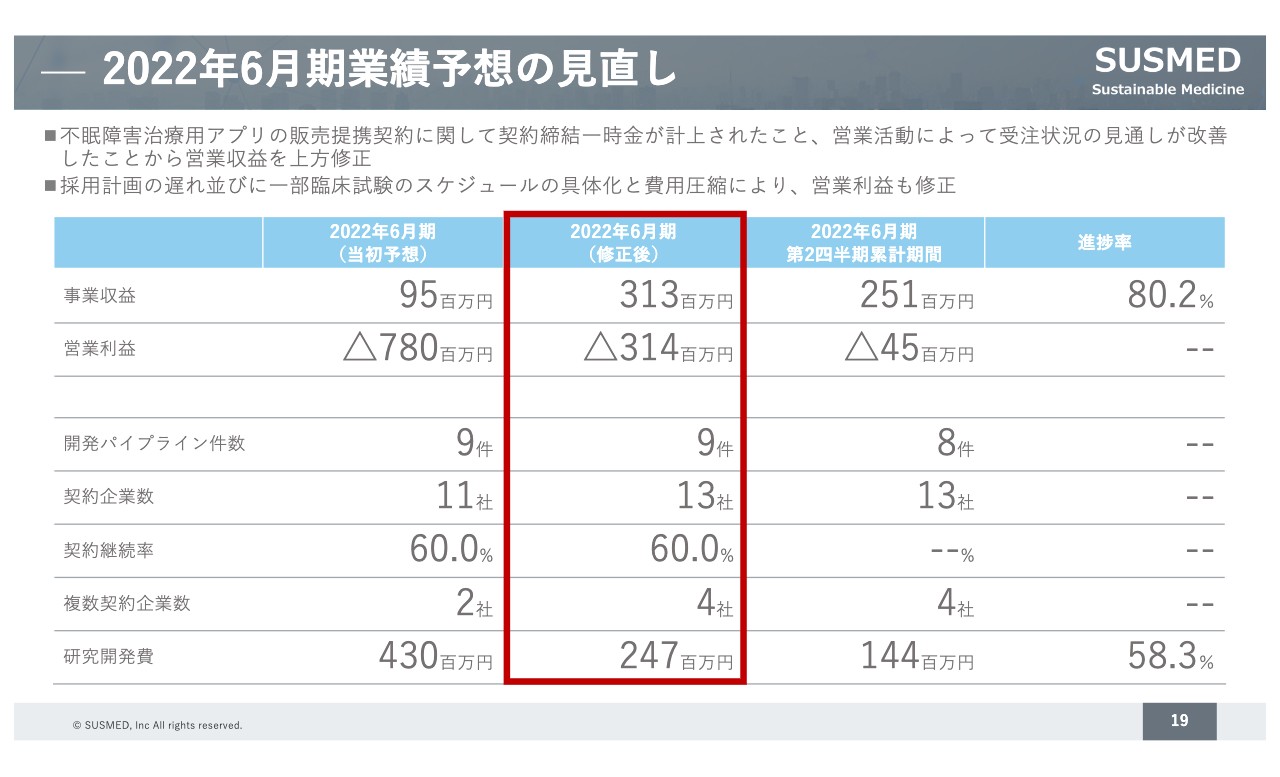
2022年6⽉期業績予想の⾒直し
これらを受け、今期の業績予想を修正しています。当初、事業収益は9,500万円と予想していましたが3億1,300万円に修正しています。営業利益は7億8,000万円の赤字を予定していましたが、赤字の圧縮が可能となったため、3億1,400万円の赤字での着地を予定しています。
研究開発費についても費用圧縮ができたことから、当初4億3,000万円を見込んでいた部分が、2億4,700万円という状況になっています。私からのご説明は以上です。
質疑応答:パイプライン承認申請のタイミング、契約企業数の推移、「SUSMEDシステム」の本格的な治験時期について
質問者1:3点おうかがいします。不眠症の治療アプリは申請に入られましたが、それ以外のパイプラインの申請については、現状、どのくらいのタイミングをお考えでしょうか?
2つ目は契約企業について、今年は予想よりは増えていますが、先ほどの表を見ると、去年より契約企業数が減っているように見えます。どのような原因で契約が取りやめになっているのか教えてください。
3つ目は「SUSMEDシステム」についてですが、今のところ、どちらかと言うと研究的な意味合いが強いと思います。これが実際に臨床現場、例えば、シミックやEPSで本格的に治験として使われるのはどのタイミングなのか教えてください。
上野:まず、「SUSMEDシステム」の状況について背景をご説明します。2年前の年末に、省庁から、私どものブロックチェーン技術を使った場合は、人手をかけたデータの照合作業を行わなくてもよいと正式に通知いただいており、それをもって治験対応できる状況になっています。
昨年の4月から、実際にAMEDのプロジェクトを東京医科歯科大学と開始し、それ以降、EPSとの業務提携や、先日の東北大学との共同研究をリリースしています。実際の治験での使用についてはまだ開示できませんが、現在すでに複数社と話が進んでいるため、そちらも開示できる状況になりましたら、速やかに共有させていただきたいと考えています。
契約件数についてはご指摘のとおりで、昨年の時点では契約企業数16社でした。先ほどの機械学習のAIの仕組みで、医療以外のドメインでの使用例がありましたが、一方で、私どもの強みとして、医療分野やドメイン知識にシナジーがあると考えているため、やはり医療分野に注力しようというところもあります。
したがって、当時医療分野以外でご使用いただいていた方々に対しては、優先順位を下げさせていただいたことが背景になっています。
パイプラインの予定については、ご指摘のように、不眠障害の治療用アプリはすでに承認申請を完了しています。後続のパイプラインの承認申請がどのタイミングになるかについては、明確にはお話しできません。
理由は、PMDAとの協議であったり、その協議のもとで治験のプロトコルが固まり、治験の観察期間や組入患者数などが確定することによって、その治験の期間等が変わってくるためです。そのような意味で、現時点で承認申請のタイミングまで明確に言えるものは、不眠障害の治療用アプリ以外はありません。
一方で、PMDAとの協議についてはそれぞれ進めており、少しずつ具体化してきている状況です。
質問者1:追加で教えていただきたいのですが、プロトコルが固まってから、協議が進み、データが正しいと確認されて申請できるまでに、どれくらいの時間を考えておけばよろしいですか?
上野:当社の不眠障害の治療用アプリを例に申し上げますと、今回、2月1日に承認申請していますが、PMDAとの協議はそれよりもかなり前から行っています。PMDAとプロトコル相談を行い、内容に合意して、実際に私どもが不眠障害の治療用アプリの検証的試験を開始したのは昨年の春です。
その後、昨年の11月まで治験を実施しポジティブな結果が出たため、承認申請の準備を実施しましたが、そこから実際に申請するまでに2ヶ月強かかっています。承認申請の準備と並行してPMDAに申請前の事前相談をさせていただき、問題ないことを確認した上で、2月1日に承認申請という流れになっています。
質疑応答:パイプライン全体における交渉の状況について
質問者2:パイプライン全体では、いわゆる大手企業からの引き合いにおいて現段階では出さず、塩野義製薬に出したように最後まで行った上でよい条件を取るのでしょうか? ライセンスアウト的な交渉の現状を、お話しできる範囲で教えてください。
上野:スライドに掲載しているパイプラインに限らず、製薬企業の方々に治療用アプリに非常に強い関心をいただいており、話をしているところです。
あとはタイミングです。おっしゃるとおり、不眠障害治療用アプリは承認申請まで私どもで完了し、販売の部分で塩野義製薬さまと提携しています。早期に導出するよりも、むしろ後のほうが私どもとしても企業価値を最大化できると考えています。
もちろんパイプラインの種類によって、開発におけるシナジーが見込まれることがあれば、不眠障害治療用アプリの前例に限ったかたちではなくてもよいと考えています。
私どもは、このような治療用アプリの開発ノウハウや蓄積に加え、さらにブロックチェーンとのシナジーも、非常にあると考えています。普通にCROの方々に治験を実施いただく場合は、非常に大きなコストがかかってしまいますが、ブロックチェーンの治験システムを活用することで研究開発費を圧縮し進めることができます。一般的なバイオベンチャーのように、開発のコストが重いため早期に導出することは必ずしも必要ないのが強みだと考えています。
質疑応答:塩野義製薬からの一時金について
質問者2:塩野義製薬から、一時金として2億円受領していると思います。一方で、リリースのとおりだとディールの総額自体は47億円だと思います。今回の条件やロイヤリティ率、販売マイルストーンも含んだ額なのか、今後お金がどのように入ってくるか、イメージだけでも教えていただけないでしょうか?
上野:販売後のレベニューシェアもありますし、販売のマイルストーンもいろいろな段階があると思いますが、今回はあくまでも契約一時金として2億円のみ受領している状況です。
私どもはプロダクトに自信があることもあり、一時金としては2億円だけで、後に残りの45億円いただくような契約をしているのが正直なところです。販売のレベニューシェアは、別途いただくかたちをとっています。
質問者2:ロイヤリティ率については言及できますか? いわゆる普通の医薬品だと少なくとも2桁以上、20パーセント、30パーセント以上が、フェーズ3のあとの導出だと思いますが、ヒントだけでもいただけるものはあるでしょうか?
上野:先方との都合もあり開示は控えますが、おっしゃっていただいたように、早期に導出しているものではなく、あくまで販売提携で協業しています。早期の導出とは違うということは、お伝えしておきたいと思います。
質疑応答:分散型治験について
質問者2:最近ブロックチェーン関連で、新型コロナウイルスに関連して「分散型治験」というワードをよく見かけるようになりました。
御社のシステムは、病院に行かなくてもいろいろなデータを取れるような、CROの業務負担の軽減以外でも活きるシステムであり、シナジーが生まれるのでしょうか? または、別にDCT(Decentralized Clinical Trial)はブロックチェーンなどがなくても、どうにか回っている状況でしょうか? 現状をわかる範囲でご説明いただきたいです。
上野:おっしゃるとおり、分散型治験やRemote Clinical Trialというような、医療機関を受診しなくても治験に参加できるようにする方法は、新型コロナウイルスの影響でニーズが高まっている状況だと思います。
私どもは、もともとスマートフォンの治療用アプリ経由で患者さんのデータを集め、そちらのデータを医療機関やCROに共有する仕組みを持っているため、リモートでの臨床試験を実施できます。
さらに、ブロックチェーンの技術を加えることにより、これまで実地で、人の目でチェックしなければレギュレーション対応できなかった部分が、システムでできるようになりました。治験業務自体を医療機関に行かないというリモートだけではなく、いわゆる分散型治験やRemote Clinical Trialのさらにもう一歩先の、そもそも人がチェックする必要がないというシステムです。
いわゆる「Web3」の文脈でいわれているような、システムによるデータの信頼性の担保までできるのが、私どもの強みだと思います。分散型治験も、従来どおりスマートフォン経由でデータ取得というところでは対応しています。
質疑応答:不眠障害治療用アプリについて
質問者3:不眠障害治療用アプリについての市場戦略の考え方を、もう一度教えていただけますか?
上野:不眠障害自体が非常にいわゆるコモンディジーズで、日本国内で1,860万人の不眠症状を訴える方がいるといわれています。
そのうち、現時点で睡眠薬の処方を受け治療している方が、日本国内に590万人いるといわれています。したがって、ファーストターゲットはすでに睡眠薬による治療を受けている590万人になりますが、一方でギャップの部分の1,200万人は、不眠症状を抱えながらも治療を受けていない方々です。
そのような方々は、睡眠薬を飲みたくないために治療を受けない、あるいは薬局で処方箋なしで使えるOTC薬を使ったり、場合によっては寝酒などで対応されたりしている方々がいらっしゃいます。そのような方々は潜在的なユーザーになると考えており、次のマーケットだと考えています。
質問者3:塩野義製薬とのお話は、残りの45億円は販売前にもらえるマイルストーンということですか?
上野:ロイヤリティは別ですが、販売中のマイルストーンも含めています。
質疑応答:塩野義製薬側のメリットについて
質問者3:塩野義製薬は御社と組むことにより、何を得ることができるのでしょうか?
上野:不眠障害は、さまざまな精神疾患のリスクファクターになることがあります。例えばうつ病患者は不眠症状を併発したり、不眠症状から始まってうつの状態になったりします。
私個人の考えのため、正確には塩野義製薬さまに確認していただきたいですが、塩野義製薬さまは非常に有名な「サインバルタ」という抗うつ薬を販売しています。そちら以外にも、抗うつ薬の開発を精力的に進められていると思います。そのような意味で、疾患領域でのシナジーが非常にあると考えています。